
 ,故答案为:
,故答案为: ;
;
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、c(H+)>c(A-) |
| B、c(H+)>c(HA) |
| C、c(OH-)>c(HA) |
| D、c(HA)>c(A-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
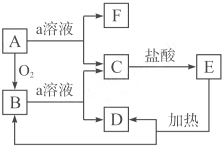 如图,A是一种非金属单质,E是一种白色沉淀.据图填空:
如图,A是一种非金属单质,E是一种白色沉淀.据图填空:查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/s | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)/mol?L-1 | 0.100 | c1 | 0.050 | c3 | c3 |
| c(NO2)/mol?L-1 | 0.00 | 0.060 | c2 | 0.120 | 0.120 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式
(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式
|
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com