
| A. | 加入少量的KCl固体 | B. | 加入少量FeCl3固体 | ||
| C. | 降低Fe(SCN)3的浓度 | D. | 加水稀释 |
分析 A、根据实际参加反应的离子浓度分析,加入少量KCl固体,溶液中Fe3+、SCN-浓度不变;
B、加入少量氯化铁固体,溶液中Fe3+浓度增大,平衡正向进行;
C、平衡是水溶液中的平衡,减少Fe(SCN)3的浓度,平衡正向进行;
D、结合平衡常数分析,加水稀释,离子浓度降低,反应物浓度系数次幂的乘积降低更多.
解答 解:A、根据实际参加反应的离子浓度分析,化学平衡为Fe3++3SCN-=Fe(SCN)3,加入少量KCl固体,溶液中Fe3+、SCN-浓度不变,平衡不动,故A错误;
B、加入少量氯化铁固体,溶液中Fe3+浓度增大,平衡正向进行,故B错误;
C、减少Fe(SCN)3的浓度,平衡正向进行,故C错误;
D、加水稀释,离子浓度降低,溶液颜色变浅,c3(SCN-)•c(Fe3+)降低更多,平衡逆向移动,故D正确;
故选D.
点评 本题考查化学平衡的影响因素分析判断,注意建立平衡的微粒分析应用,掌握基础是关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N、P、As的电负性随原子序数的增大而增大 | |
| B. | 价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素 | |
| C. | 2p和3p轨道形状均为哑铃形,能量也相等 | |
| D. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2 | B. | HCl | C. | Ba(OH)2 | D. | NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如表和如图表示:下列说法正确的是( )
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如表和如图表示:下列说法正确的是( )| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5molA 0.5molB | 1.5molA 0.5molB | 6.0molA 2.0molB |
| A. | 10min内甲容器中反应的平均速率v(A)=0.025mol/(L•min) | |
| B. | 由图可知:T1<T2,且该反应为吸热反应 | |
| C. | x=1,若平衡时保持温度不变,改变容器体积平衡移动 | |
| D. | T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为75% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| X | Y | Z | |
| W | |||
| T |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验现象 | 结论 | |
| ① | 通电后,铁棒和石墨棒上都有气泡冒出 | |
| ② | 将阴极上方收集的气体靠近火焰,有爆鸣声 | |
| ③ | 阳极收集到的气体呈黄绿色,可使湿润的淀粉KI试纸变蓝 | |
| ④ | 铁棒一端的溶液滴加酚酞后变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
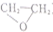 )的反应中,原子利用率最高的是( )
)的反应中,原子利用率最高的是( )| A. | CH2═CH2+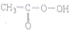 (过氧乙酸)→ (过氧乙酸)→ +CH3COOH +CH3COOH | |
| B. | CH2═CH2+Cl2+Ca(OH)2→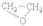 +CaCl2+H2O +CaCl2+H2O | |
| C. | 2CH2═CH2+O2$\stackrel{催化剂}{→}$2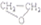 | |
| D. |  $\stackrel{催化剂}{→}$ $\stackrel{催化剂}{→}$ +HOCH2CH2-O-CH2CH2OH+2H2O +HOCH2CH2-O-CH2CH2OH+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com