
以下自发反应能用△H判据来解释的是
A.硝酸铵自发地溶于水
B.2N2O5(g) = 4NO2 (g) + O2(g) △H = + 156.7kJ/mol
C.(NH4)2CO3(s) = NH4HCO3(s) + NH3(g) △H =+74.9 kJ/mol
D.2H2(g) + O2(g) = 2H2O(l) △H =-285.8kJ/mol
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
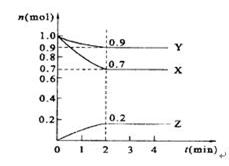
(1)X的转化率是
(2)由图中所给数据进行分析,该反应的化学方程为 ;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)= ,
(4)当反应进行到第 min,该反应达到平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既属于氧化还原反应,又属于吸热反应的是
A.铝片与稀盐酸反应 B.甲烷在氧气中燃烧
C.灼热的炭与二氧化碳反应 D.Ba(OH)2·8H2O与NH4Cl反应
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定量的密闭容器中进行反应:N2(g)+3H2 2NH3(g)。已知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1 mol/L、0.3 mol/L、0.2 mol/L。当反应达到平衡时,可能存在的数据是
2NH3(g)。已知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1 mol/L、0.3 mol/L、0.2 mol/L。当反应达到平衡时,可能存在的数据是
A.N2为0.2 mol/L,H2为0.6 mol/L B.N2为0.15 mol/L
C.N2、H2均为0.18 mol/L D.NH3为0.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备纯硅反应的化学方程式为SiCl4(g) + 2H2(g)  Si(s) + 4HCl(g) △H>0,下列措施能提高反应速率且使平衡向正反应方向移动的是
Si(s) + 4HCl(g) △H>0,下列措施能提高反应速率且使平衡向正反应方向移动的是
A.升温 B.加压 C.减压 D.加催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示的装置进行实验:
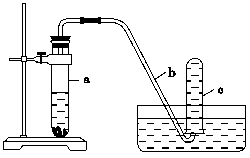
(1)在实验开始前必须先做的实验操作是
(2)向试管a中加入10 mL6 mol/L的稀HNO3和1 g Cu片,立即用带有导管的橡皮塞塞紧试管口,请写出在试管a中有可能发生的反应的化学方程式
_________________________________________________________________________________________________________________________________________________________。
(3)实验过程中常常反应开始时速率缓慢,随后逐渐加快,这是由于_______ _________,当反应进行一段时间后速率又逐渐减慢,原因是 _。
(4)欲较快地制得NO,可采取的措施是________。
A.加热 B.使用铜粉 C.稀释HNO3 D.改用浓HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是
A.含有共价键的化合物是共价化合物 B.含有离子键的化合物是离子化合物
C.共价化合物可能含有离子键 D.离子化合物不可能含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。实验所用仪器如下:

(1)写出发生装置中进行反应的化学方程式: ;
(2)上述仪器的连接顺序是(填接口字母):E接 , 接 , 接 , 接 。
(3)实验前,应该进行的一项操作是 。
(4)饱和食盐水的作用是 。
(5)若实验中得到标况下11.2L氯气,被氧化的HCl的物质的量为 ,此时转移的电子数是 。
(6)下列试剂中,可以用来吸收残余氯气的是 。
A.饱和食盐水 B.氢氧化钠溶液 C.碳酸钠溶液 D.浓硫酸
(7)工业上制取氯气的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
右图为元素周期表短周期的一部分。关于A~G 七种元素的叙述正确的是
A.E、F、G形成的单质中都含有共价键
B.形成的简单阴离子半径:E > C > D
C.B、C、D三种元素的氢化物的稳定性依次减弱
D.A、B、E的氢化物都能跟HNO3 发生化合反应

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com