
铁和稀硫酸在敞口容器中进行反应: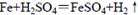 ,下列叙述中不正确的是
,下列叙述中不正确的是
A.该反应的反应过程与能量关系可以用下图表示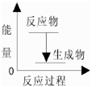 |
| B.若将该反应设计成原电池,当正极产生22.4L气体时,有56g铁溶解 |
| C.若将该反应设计成原电池,溶液中SO42-向Fe电极移动 |
| D.若将该反应设计成原电池,负极发生的反应是:Fe -2e =Fe2+ |
科目:高中化学 来源: 题型:单选题
在25 ℃、101 kPa下,1 g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68 kJ,下列表示甲醇燃烧热的热化学反应方程式是
A.CH3OH(l) + O2(g)=CO2(g)+2H2O(l)△H=+725.8 kJ·mol-1 O2(g)=CO2(g)+2H2O(l)△H=+725.8 kJ·mol-1 |
| B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452 kJ·mol-1 |
C.CH3OH(l) + O2(g)=CO2+2H2O△H=-725.8 kJ·mol-1 O2(g)=CO2+2H2O△H=-725.8 kJ·mol-1 |
D.CH3OH(l) + O2(g)=CO2(g)+2H2O(l)△H=-725.8 kJ·mol-1 O2(g)=CO2(g)+2H2O(l)△H=-725.8 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知2H2(g)+O2(g)→2H2O(g)+483.6kJ。下列说法或表达正确的是
| A.在相同的条件下,2mol 氢气与 1 mol 氧气的总能量小于2mol 水蒸气的总能量 |
| B.H2(g)+1/2 O2(g)→H2O(1)+Q1;Q1>241.8kJ |
| C.H2(g)+ 1/2O2(g)→H2O(1)+Q2;Q2<241.8kJ |
| D.任何条件下,2L水蒸气分解成2L氢气与1L氧气需吸收483.6kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知:H2(g) + F2(g) = 2HF(g) ΔH=? 270 kJ/mol,下列说法正确的是
| A.在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 |
| B.1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ |
| C.该反应的逆反应是放热反应 |
| D.该反应过程的能量变化可用下图来表示 |
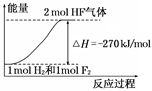
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3一kJ/mol、2800 kJ/mol。则下列热化学方程式正确的是
A.C(s)+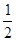 O2(g)=CO(g);△H=" -" 393.5 kJ/mol O2(g)=CO(g);△H=" -" 393.5 kJ/mol |
| B.2H2(g)+O2(g)=2H2O(l);△H="+571.6" kJ/mol |
| C.CH4(g)+CO2(g)=CO2(g)+2H2O(g);△H=-890.3 kJ/mol |
D.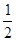 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H="-1400" kJ/mol C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H="-1400" kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述不正确的是
| A.纯银器表面在空气中因化学腐蚀渐渐变暗 |
| B.氢氧燃料电池是一种将化学能转化为电能的装置 |
| C.可用浸有酸性高锰酸钾溶液的滤纸来检验二氧化硫气体的漂白性 |
| D.塑料袋在全球“失宠”,有偿使用成为风尚,是因为塑料袋填埋占用土地,且难以降解 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中正确的是
| A.化学反应中的能量变化,表现形式除热量外还可以是光能和电能等 |
| B.化学反应中的能量变化不一定服从能量守恒定律 |
| C.在一个确定的化学反应关系中,反应物的总能量与生成物的总能量可能相同 |
| D.在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上也可以用CO2和H2反应制得甲醇。在2×105Pa、300℃的条件下,若有44g CO2与6g H2恰好完全反应生成气体甲醇和水,放出49.5kJ的热量。试写出该反应的热化学方程式: 。
某次实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。
试回答下列问题: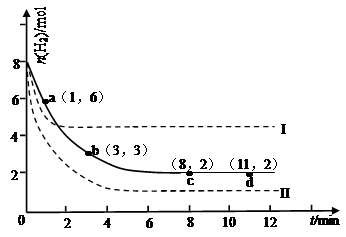
(1)a点正反应速率 (填大于、等于或小于)逆反应速率。
(2)下列时间段平均反应速率最大的是 ,最小的是 。
| A.0~1min |
| B.1~3min |
| C.3~8min |
| D.8~11min |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com