
在容积可变的密闭容器中,充入适量X与Y的混合气,一定条件下发生反应:X(气)+3Y(气) =2Z(气)若维持温度与压强不变,达平衡时,容器容积为VL,其中Z占10%,下列推断中,正确的是
A.原X、Y 混合气体积为1.2VL B.原X、Y混合气体积为1.1VL
混合气体积为1.2VL B.原X、Y混合气体积为1.1VL
C.达平衡时,消耗X体积为0.25VL D.达平衡时,消耗Y体积为0.05VL
科目:高中化学 来源:2016-2017学年云南省高一上期中化学试卷(解析版) 题型:选择题
将某二价金属的氧化物4g还原为金属单质,需0.2mol电子,则该金属元素的相对原子量为( )
A 24 B 40 C 56 D 64
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学试卷(解析版) 题型:选择题
下列各对物质中,互为同系物的是
A.CH3—CH3 和CH3—CH=CH2
B.CH3—CH=CH2 和 CH2—CH2—CH=CH2
C.CH3—CH2—CH3 和CH3—CH=CH2
D.CH3—CH2CH2—CH3 和 CH3—CH2—OH
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
某学生用碱式滴定管量取NaOH溶液,开始时仰视液面,读数为5.00 mL,取出部分溶液后,俯视液面,读数为15.00 mL,该同学在操作中实际取出的液体为
A.大于10.00 mL B.小于10.00 mL C.等于10.00 mL D.等于11.00 mL
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
H2S水溶液中存在电离平衡H2S H++HS– 和HS–
H++HS– 和HS– H++S2–,下列说法正确的是
H++S2–,下列说法正确的是
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入适量SO2气体,平衡向右移动,溶液pH值减小
C.滴加新制氯水,平衡向左移动,溶液pH值减小
D.加入少量烧碱固体(忽略体积变化),溶液中所有离子浓度都减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上期中化学卷(解析版) 题型:推断题
软质隐形眼镜材料W、树脂X的合成路线如图所示。

(1)A中含有的官能团的结构简式是_______________。
(2)甲的结构简式是_______________。
(3)B→C反应的化学方程式是____________________________。
(4)B有多种同分异构体.属于酯且含有碳碳双键的同分异构体共有______________种(不考虑顺反异构。
(5)已知F的相对分子质量为110,1molF可与足量钠反应生成22.4L氢气(标准状况下),
苯环上的氢原子化学环境都相同.则F还能发生的反应是 _______________(填序号)
_______________(填序号)
a.加成反应 b.氧化反应 c.加聚反应 d.水解反应
(6)写出树脂X可能的结构简式_______________(写出一种即可)。
(7)E的分子式为C10H14O2,含三个甲基,苯环上的一溴代物有两种,生成E的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上期中化学卷(解析版) 题型:选择题
已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如下:
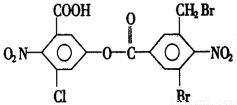
1mol该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为a(不考虑醇羟基和硝基与氢氧化钠的反应,下同),溶液蒸干得到的固体产物再与足量的干燥碱石灰共热,又消耗氢氧化钠的物质的量为b,则a,b分别是( )
已知: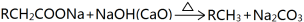
A.5mol,10mol B.6mol,2mol C.8mol,4mol D.8mol,2mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上期中化学卷(解析版) 题型:实验题
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是 ;
(2)要加快上述实验中气体产生的速率,还可采取的措施有: 、 (答两种);
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
实验 混合溶液 | A | B | C | D | E | F |
4mol/L H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
① 完成此实验设计,其中:V1= ,V6= ,V9= ;
完成此实验设计,其中:V1= ,V6= ,V9= ;
②同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因  。
。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学卷(解析版) 题型:选择题
t℃时,某平衡体系中含有X、Y、Z、W四种物质,此温度下发生反应的平衡常数表达式为: 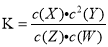 。有关该平衡体系的说法正确的是
。有关该平衡体系的说法正确的是
A.升高温度.平衡常数K一定增大
B.增大压强.W(g)质量分数增加
C.升高温度.若混合气体的平均相对分子质量变小.则正反应是放热反应
D.增大X(g)浓度.平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com