
A.常温下,浓H2SO4与铁、铝不反应,所以铁质、铝质容器能盛放浓H2SO4
B.浓H2SO4具有吸水性,能使蔗糖炭化
C.浓H2SO4和铜片加热既表现出酸性,又表现出氧化性
D.浓H2SO4与亚硫酸钠反应制取SO2时,浓H2SO4表现出强氧化性
解析:(1.)常温下浓H2SO4与铁、铝接触,能使金属表面生成一层致密的氧化物保护膜,阻止内部金属继续跟硫酸反应。并不是Fe、Al与浓H2SO4不反应。
(2)浓硫酸从蔗糖中夺取与水分子组成相当的氢和氧,使蔗糖炭化,体现了浓硫酸的脱水性而不是吸水性。
(3)铜与浓H2SO4在加热条件下发生反应,其方程式为:
![]()
![]()
![]()
反应中浓H2SO4为氧化剂,铜为还原剂,氧化剂与还原剂的物质的量之比为1∶1。因每反应掉2 mol浓H2SO4,1 mol作氧化剂,还有1 mol起酸的作用。
(4)实验室中是用浓H2SO4与固体亚硫酸钠反应来制取二氧化硫的:
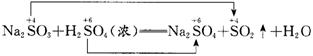
在反应物中硫元素处于相邻价态,根据氧化还原反应规律知,它们之间是不可能发生氧化还原反应的,应为复分解反应,其原理是用难挥发性酸制易挥发性酸,强酸制弱酸。因而在此反应中浓H2SO4表现的是难挥发性和酸性。
答案:C


科目:高中化学 来源: 题型:
| A、常温下,浓H2SO4与铁、铝不反应,所以铁、铝质容器能盛装浓H2SO4 | B、浓H2SO4具有吸水性,能使蔗糖炭化 | C、浓H2SO4和铜片加热既表现强酸性,又表现强氧化性 | D、浓H2SO4和Na2SO3反应制取SO2时,浓H2SO4表现出强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.常温下,浓H2SO4与铁、铝不反应,所以铁质、铝质容器可盛放浓H2SO4
B.浓硫酸具有吸水性,能使蔗糖炭化
C.浓硫酸和铜片加热既表现强酸性,又表现出强氧化性
D.浓硫酸与亚硫酸钠反应制取二氧化硫时,浓H2SO4表现出强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
A.常温下,浓H2SO4与铁、铝不反应,所以铁质、铝质容器能盛放浓H2SO4?
B.浓H2SO4具有吸水性,能使蔗糖碳化?
C.浓H2SO4和铜片共热既能表现H2SO4的酸性,又表现出强氧化性?
D.浓H2SO4与亚硫酸钠反应制取SO2时,浓H2SO4表现出强氧化性?
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对浓H2SO4的叙述正确的是( )
A.常温下,浓H2SO4与铁、铝不反应,所以铁质、铝质容器能盛放浓H2SO4
B.浓H2SO4具有吸水性,能使蔗糖炭化
C.浓H2SO4和铜片共热,H2SO4既能表现出酸性,又能表现出强氧化性
D.浓H2SO4与亚硫酸钠反应制取SO2时,浓H2SO4表现出强氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com