
【题目】己知某溶液中只存在OH-、H+、NH4+、CL-四种离子,某同学推测其离子浓度大小顺序可能有如下四种关系:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-)
②c(NH4+)>c(OH-)>c(Cl-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
⑴若溶液中只有一种溶质,则该溶质是_________________。
⑵若四种离子的关系符合③,则溶质为___________;若四种离子的关系符合④,则溶质为________。
⑶将pH相同的NH4Cl溶液稀释相同的倍数,下面图像正确的是(填图像序号)______________。

【答案】(1)NH4C1(2)NH4C1和NH3·H2O;NH4C1和HC1(3)B
【解析】
试题分析:(1)因任何水溶液中都有OH-、H+,若溶质只有一种则为NH4Cl;
(2)由③中离子的关系可知溶液显碱性,且c(NH4+)>c(Cl-),则溶液为氯化铵和氨水的混合溶液,其溶质为NH4Cl和NH3·H2O;(四种离子浓度关系有c(Cl-)>c(H+)>c(NH4+) > c(OH-),说明溶液显酸性,氯离子浓度大于铵根,所以是氯化铵和氯化氢的混合溶液;
(3)pH相同的NH4Cl溶液和HCl溶液稀释时氢离子的浓度都变小,则pH都变大,但盐酸为强电解质,则pH变化程度大,而氯化铵水解显酸性,稀释促进水解,氢离子浓度减小的倍数小于盐酸中氢离子浓度的变化,则pH变化小,只有B符合题意,答案选B。


科目:高中化学 来源: 题型:
【题目】在25℃时,将amol/L的氨水与0.01mol/L的HCl溶液等体积混合,反应后溶液呈中性,下列说法不正确的是(忽略溶液混合后体积的变化)
A.溶液中c(NH4+)=c(Cl-)
B.此时水的电离程度最大
C.此时溶液中NH3·H2O的物质的量浓度为1/2[(a-0.01)]mol/L
D.用含a 的代数式 NH3·H2O的电离平衡常数Kb=![]() (mol/L)
(mol/L)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若mgNa在足量氯气中燃烧,生成固体的质量为(m+3.55)g,则mgNa与氧气反应,生成固体的质量为( )
①(m+0.8)g ②(m+1.0)g ③(m+1.2)g④(m+1.6)g ⑤(m+1.4)g
A.①④
B.①⑤
C.③④
D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。该电池是以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液,其总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列说法正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列说法正确的是
A.Zn为电池的正极
B.充电时阳极反应为:Fe(OH)3-3e+5OH =FeO42-+4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.该电池放电过程中电解质溶液浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、恒压下,a mol A和b mol B在一个容积可变的容器中发生反应:A(g)+2B(g) ![]() 2C(g),一段时间后达到平衡,生成n mol C。则下列说法中正确的是
2C(g),一段时间后达到平衡,生成n mol C。则下列说法中正确的是
A.物质A、B的转化率之比为a∶b
B.起始时刻和达平衡后容器中的压强之比为(a+b)∶(a+b-n/2)
C.若起始时放入2 a mol A和2b mol B,则达到平衡时生成2nmol C
D.当2V正(A)=2V逆(B) 时,可证明反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是
A.使酚酞变红色的溶液中:Na+、Al3+、S2-、Cl-
B.无色透明的溶液中:K+、Cu2+、Cl-、NO3-
C.0.1 mol·L-1NH4HCO3溶液中:K+、Na+、NO3-、Cl
D.常温下![]() =1012的溶液:Fe2+、I-、NO
=1012的溶液:Fe2+、I-、NO![]() 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等。
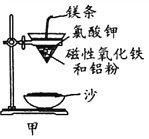
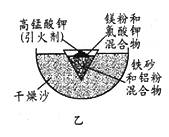
(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观。指明使用镁条和氯酸钾的目的是 ______________________。
(2)某同学用图乙装置进行铝热反应。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见血红色。为测定该实验所得 “铁块”中铁元素含量,设计实验流程如图所示。
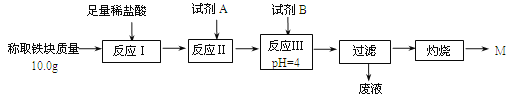
几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
Fe2+ | Fe3+ | Al3+ | Mg2+ | |
开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
① 试剂A应选择________,试剂B应选择_______。(填序号)
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水
② 写出反应Ⅱ的离子方程式_____________________。
③ 设计简单实验证明M的成分是Fe2O3而非Fe3O4。
操作 | 预期现象 |
取少量M固体于试管中,向其中加入________________;观察。 | 固体完全溶解,溶液呈黄色。 |
继续向上述溶液中滴入_________________,振荡观察 | ______________________ |
④ 上述实验应灼烧至M质量不变,则能证明M质量不变的标志是____________。
⑤ 若最终红色粉未M的质量为12.0 g,则该“铁块”的纯度是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】长征2号火箭承担运载“神六”的使命,氕化锂、氘化锂、氚化锂可以作为启动长征2号(CZ2F)火箭的优良炸药。下列说法正确的是
A. LiH、LiD、LiT的摩尔质量之比为1∶2∶3 B. 它们都是强还原剂
C. H、D、T之间互称为同素异形体 D. 它们都是强氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】西安北郊古墓中曾出土一青铜锤(一种酒具),表面附着有绿色固体物质,打开盖子酒香扑鼻,内盛有26 kg青绿色液体,专家认定是2000多年前的“西汉美酒”。这是我国考古界、酿酒界的一个重大发现。
(1)上述报道引发了某校化学兴趣小组同学的关注,他们收集家中铜器表面的绿色固体进行探究。
提出问题:铜器表面附着绿色固体物质是由哪些元素组成的?
猜想:查阅相关资料后,猜想绿色固体物质可能是铜绿。
实验步骤:

①对试管内的绿色固体进行加热,至完全分解。观察到A装置中绿色固体逐渐变成黑色,B装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊。
②取少量加热后生成的黑色固体于试管中,加入稀硫酸。观察到黑色固体逐渐溶解,溶液变成蓝色。
③取少量上述蓝色溶液于试管中,浸入一根洁净的铁丝。观察到铁丝表面有红色物质析出。
④实验结论:绿色固体物质中含有________、________、________、________等元素(用元素符号作答)。(提示:装置内的空气因素忽略不计)
(2)表达与交流
①上述实验步骤③中发生反应的离子方程式________________________。
②干燥管中的碱石灰作用是什么? _。
若反应结束后,如果先移去酒精灯,可能出现的现象是什么? _。
③如果将B、C两装置对调行吗?________。为什么? _____ _______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com