
【题目】氢能是一种极具发展潜力的清洁能源。
(1)氢气的制取与储存是氢能源利用领域的研究热点.
已知:①CH4的燃烧热为890KJ·mol-1; ②H2的热值为50.2kJ·g-1
则甲烷部分氧化生成CO2和H2的热化学方程式为___________________________________;该反应自发进行的条件是___________。
(2)Bodensteins研究了如下反应:2HI(g)![]() H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
X(HI) | 1.00 | 0.910 | 0.850 | 0.815 | 0.795 | 0.784 |
X(HI) | 0.00 | 0.600 | 0.730 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为:___________。
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,若k正=9.00min-1,在t=20min时,v逆=__________min-1(保留三位有效数字)
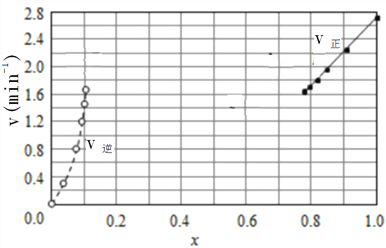
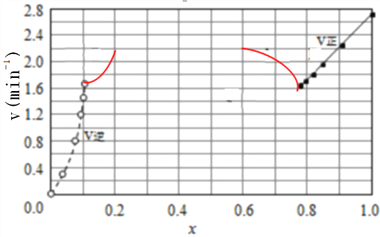
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。在上述平衡基础上,缓慢升高到某一温度,反应重新达到平衡,请在下图中画出此过程的趋势图。______________
(3)一种可超快充电的新型铝电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其它离子不参与电极反应,放电时负极Al的电极反应式为______________________。
【答案】 CH4(g)+O2(g)=CO2(g)+2H2(g) △H3=-689.2KJ·mol-1 任意条件均自发 K=0.1082/0.7842 0.960或19.0 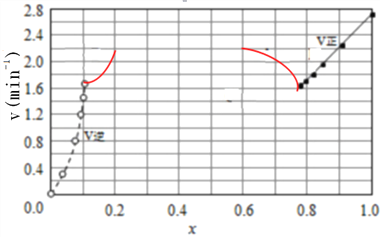 Al-3e-+7 AlCl4—==4 Al2Cl7—
Al-3e-+7 AlCl4—==4 Al2Cl7—
【解析】(1)CH4燃烧的热化学方程式:①CH4(g)+2O2(g)==CO2(g)+2H2O(l), H=-890KJ·mol-1,H2的热值为50.2kJ·g-1,反应热为100.4KJ·mol-1,热化学方程式:②H2(g)+1/2O2(g)== H2O(l), H=-100.4KJ·mol-1;根据盖斯定律:①-②×2,得CH4(g)+O2(g)=CO2(g)+2H2(g) △H3=-689.2KJ·mol-1;该反应为H<0,S>0,任意条件均自发进行反应;正确答案:CH4(g)+O2(g)=CO2(g)+2H2(g) △H3=-689.2KJ·mol-1 ;7任意条件均自发。
(2)(1)2HI(g)![]() H2(g)+I2(g)是反应前后气体物质的量不变的反应;反应后x(HI)=0.784,则x(H2)=x(I2)=0.108,K=
H2(g)+I2(g)是反应前后气体物质的量不变的反应;反应后x(HI)=0.784,则x(H2)=x(I2)=0.108,K= =
=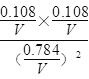 =
=![]() ;正确答案:K=0.1082/0.7842 。
;正确答案:K=0.1082/0.7842 。
(2)到达平衡时,v正=v逆,即k正x2(HI)=k逆x(H2)x(I2),k逆=k正·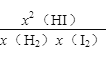 =k正/K,在t=20 min时,x(H2)= x(I2)=0.045,根据K= k正×k逆,已知k正=9.00min-1,所以k逆= k正/K=9/(0.1082÷0.7842)=473.6,v逆=k逆x(H2)x(I2)= 473.6×(0.045)2=0.96;正确答 案:0.960或19.0。
=k正/K,在t=20 min时,x(H2)= x(I2)=0.045,根据K= k正×k逆,已知k正=9.00min-1,所以k逆= k正/K=9/(0.1082÷0.7842)=473.6,v逆=k逆x(H2)x(I2)= 473.6×(0.045)2=0.96;正确答 案:0.960或19.0。
(3)原平衡时,x(HI)为0.784,x(H2)为0.108,二者图中纵坐标均约为1.6(因为平衡时v正=v逆),升高温度,正、逆反应速率均加快,对应两点在1.6上面,该反应2HI(g)![]() H2(g)+I2(g)△H=+11kJ/mol,升高温度,平衡向正反应方向移动,x(HI)减小,x(H2)增大,据此可以画出图像变化,图像如下:正确答案:
H2(g)+I2(g)△H=+11kJ/mol,升高温度,平衡向正反应方向移动,x(HI)减小,x(H2)增大,据此可以画出图像变化,图像如下:正确答案:
(3)放电时为原电池,金属铝做负极被氧化,根据电子守恒和电荷守恒规律,该极反应为:Al-3e-+7 AlCl4—==4 Al2Cl7—;正确答案:Al-3e-+7 AlCl4—==4 Al2Cl7—。


科目:高中化学 来源: 题型:
【题目】以铬铁矿为原料![]() 可制备K2Cr2O7和金属铬。实验流程如下:
可制备K2Cr2O7和金属铬。实验流程如下:
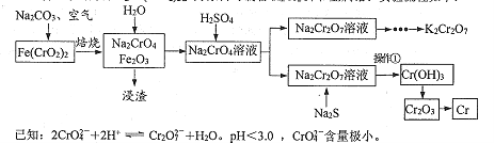
(1)写出铬铁矿焙烧转化为NazCrO4的化学反应方程式:__________________。焙烧时不能使用陶瓷容器的原因是___________________。
(2)加入稀硫酸后所得Na2Cr2O7溶液的pH 应小于3.0,可用 ____测定溶液pH。
(3)操作①包括过滤和洗涤。实验室洗涤沉淀的操作是_________________。
(4) Na2S的作用是调节溶液的酸碱度和__
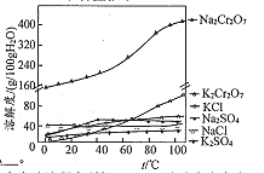
(5)Fe3+在pH为3.7时可完全转化为Fe(OH)3。在上述流程中所得NazCrz07溶液中含有少量Fe3+。请结合上图有关物质的溶解度曲线,设计由Na2Cr2O7液制备K2Cr2O7固体的实验方案(实验中须选用的试剂:硫酸、NaOH溶液、KCl固体、蒸馏水):_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室配制 500mL 0.2mol/L 的 NaOH溶液,在下图所示仪器中,配制上述溶液肯定不需要的是____(填序号),除图中已有仪器外, 配制上述溶液还需要的玻璃仪器是____。

具体过程如下:
①计算需要称量 NaOH 固体的质量_____;
②用少量蒸馏水洗涤烧杯内壁 2~3 次,洗涤液也都注入容量瓶,轻轻晃动容量瓶,使溶液混合均匀;
③用托盘天平称量 NaOH 固体;
④将 NaOH 溶液沿玻璃棒注入_____中;
⑤将称好的 NaOH 固体放入烧杯中,用适量蒸馏水溶解,并____________;
⑥盖好瓶塞,反复上下颠倒,摇匀;
⑦将蒸馏水注入容量瓶,液面离刻度线下_____cm 时,改用_______滴加蒸馏水至液面于刻度线相切;
试回答下列问题:
(1)填写上述过程中的空白;
(2)上述过程的正确顺序为___________(填步骤序号);
(3)使用容量瓶前必须进行的一步操作是____________;
(4)经精确测量,最后所得溶液物质的量浓度为 0.192mol/L,原因可能是____________。
A、使用滤纸称量 NaOH 固体;
B、未冷却直接转移至容量瓶,立即配好;
C、容量瓶中原来有少量蒸馏水;
D、称量时所用的砝码生锈;
E、溶解 NaOH 后的烧杯未经多次洗涤;
F、定容时俯视刻度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,由N2O和CO2组成的混合气体的密度是C2H4、N2和H2组成的混合气体密度的 2倍,则C2H4、N2和H2组成的混合气体中H2的质量分数为
A. 3/13 B. 10/13 C. 大于3/13,小于10/13 D. 3/143
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 标准状况下,4.6gNO2和N2O4的混合气体中原子数为0.3NA
B. 1mol 乙烯分子中含有的共价键数为4NA
C. 0.1mol·L-1的硫酸溶液中含H+的数量为0.2NA
D. 氢氧燃料电池中消耗11.2L氢气时转移电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了减少钢管因锈蚀造成的损失,某城市拟用如图方法保护埋在酸性土壤中的钢管。下列有关说法错误的是

A. 在潮湿的酸性土壤中钢管主要发生析氢腐蚀
B. 在潮湿的酸性土壤中金属棒M 将电子通过导线流向钢管
C. 在潮湿的酸性土壤中H+向金属棒M 移动,抑制H+与铁的反应
D. 金属棒M 与钢管用导线连接后可使钢管表面的腐蚀电流接近于零
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类的发展密不可分,以下不属于化学对人类贡献的是( )
A.药物和保健品的研制
B.指南针的发明与应用
C.新型高分子化合物的合成
D.合金材料的生产
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室以一种工业上的废渣(废渣主要含有MgCO3、MgSiO3和少量Fe、Al的氧化物)为原料,制备MgCO3·3H2O。实验流程如下图所示:

(1)为了加快废渣的酸溶速率,可采取的办法有_________(任写一点),酸溶时废渣中主要成分发生反应的离子方程式为___________________________________。
(2)加入30%H2O2的目的是__________________________________。
(3)用萃取分液的方法除去溶液中的Fe3+
萃取分液完成后,检验水相中是否含有Fe3+的最佳试剂是__________________________。
(4)室温下,除去MgSO4溶液中的A13+(使Al3+浓度小于1×10-6mol/L)而不引入其它杂质,应加入的试剂X为__________,应调节pH的范围为_________________。
已知:①Ksp[Al(OH)3]=1.0×10-33 ②pH=8.5 时,Mg(OH)2开始沉淀
(5)下图为不同反应温度下所得水合碳酸镁的X射线衍射谱图。由图可知,干燥时需控制温度范围为___________________,温度较高时MgCO3·3H2O发生转化的化学方程式为_______________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com