
| A. | 增大压强(对于气体反应),活化分子总数必然增大,故反应速率增大 | |
| B. | 温度升高,分子动能增加,减小了活化能,故反应速率增大 | |
| C. | 选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大 | |
| D. | H+和OH-的反应活化能非常小,反应几乎在瞬间完成 |
分析 A.对反应前后气体体积不变的反应,增大压强活化分子总数不变;
B.活化能是活化分子最低能量与反应分子的平均能量的差值,对于同一分子活化能是定值,升高温度活化能不改变.
C.使用催化剂降低活化能,提高反应速率;
D.酸和碱反应不需要外界做功的条件下就能发生,说明它们已经处于活跃状态,因此活化能非常小.
解答 解:A.反应前后气体体积不变的反应,增大压强,体积减小,活化分子总数不变,但活化分子浓度增大,反应速率增大,故A错误;
B.温度升高,更多分子吸收能量成为活化分子,反应速率增大,活化能不变,故B错误;
C.使用催化剂,降低活化能,使更多分子成为活化分子,反应速率增大,故C错误;
D.酸和碱反应不需要外界做功的条件下就能发生,说明它们已经处于活跃状态,因此活化能非常小,故D正确;
故选D.
点评 本题考查了化学反应速率的影响因素的判断和应用,题目难度不大,主要考查压强、温度、催化剂扥因素对平衡的影响,试题侧重基础知识的考查,培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量数为35的氯原子:${\;}_{35}^{17}$Cl | |
| B. | 14C的原子结构示意图: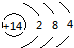 | |
| C. | N2分子的电子式: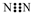 | |
| D. | 乙酸乙酯的结构简式为:CH3COOC2H5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
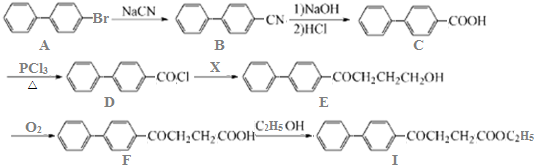
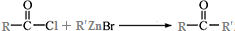
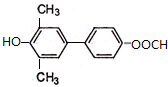 .
.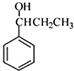 )为强效利胆药,请写出以甲苯和C2H5ZnBr为原料制备苯丙醇的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:
)为强效利胆药,请写出以甲苯和C2H5ZnBr为原料制备苯丙醇的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ |
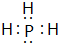 ; ⑨的最高价氧化物的对应的水化物
; ⑨的最高价氧化物的对应的水化物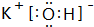 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 直线形;三角锥形 | B. | V形;三角锥形 | ||
| C. | 直线形;平面三角形 | D. | V形;平面三角形 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部由非金属元素构成的化合物一定是共价化合物 | |
| B. | 某元素的原子最外层只有一个电子,它跟卤素结合时,所形成的化学键一定是离子键 | |
| C. | 金属与非金属原子间只能形成离子键 | |
| D. | 含有共价键的化合物不一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
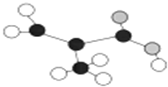
| A. | 官能团为碳碳双键、羧基 | B. | 与CH2=CHCOOCH3互为同分异构体 | ||
| C. | 能发生取代、加成和氧化反应 | D. | 分子中所有原子可能在同一平面 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com