
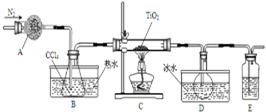
 实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.
实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产白雾 |
分析 通过氮气将装置中空气排出,防止TiCl4被氧化,A为干燥管,干燥氮气,防止生成的TiCl4遇潮湿的气体产生白雾;B装置加热使四氯化碳挥发,C中装置在加热条件下,发生反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),CCl4、TiCl4熔点较低,D装置使这两种物质转化为液态,二者能互溶,应该采用蒸馏方法分离,E装置连接空气,盛放浓硫酸,干燥空气,
(1)根据仪器的特征及常见仪器的名称解答,因为TiCl4遇到水蒸气会水解,所以E中可以用浓硫酸来隔离空气,对于气体的制取性质实验应该:组装仪器、检验气密性、加装药品,发生反应;
(2)终止实验时为防止倒吸,应先熄灭酒精灯,冷却到室温后再停止通入N2;分离两种沸点不同的液体混合物应该用蒸馏.
解答 解:通过氮气将装置中空气排出,防止TiCl4被氧化,A为干燥管,干燥氮气,防止生成的TiCl4遇潮湿的气体产生白雾;B装置加热使四氯化碳挥发,C中装置在加热条件下,发生反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),CCl4、TiCl4熔点较低,D装置使这两种物质转化为液态,二者能互溶,应该采用蒸馏方法分离,E装置连接空气,盛放浓硫酸,干燥空气.
(1)仪器A呈球形,在该实验中用于干燥氮气,为球形干燥管,因为TiCl4遇到水蒸气会水解,所以E中可以用浓硫酸来隔离空气中的水蒸汽;对于气体的制取性质实验应该:组装仪器、检验气密性,加装药品,发生反应,
故答案为:干燥管;浓硫酸;检验气密性;
(2)终止实验时为防止倒吸,应先熄灭酒精灯,冷却到室温后再停止通入N2;CCl4和TiCl4是两种沸点差异较大的液体混合物,应该用蒸馏,
故答案为:bca;防止倒吸或避免生成的产物在受热情况下与氧气反应(二者任写其一均给分);蒸馏.
点评 本题以工业流程图即物质的制取为背景,考查了实验仪器的识别、试剂的选择以及常见实验操作,锻炼了学生分析问题、解决问题的能力.


科目:高中化学 来源: 题型:解答题
 某化学兴趣小组的同学为探究二氧化硫的化学性质,设计了如图所示的装置.请回答下列问题.
某化学兴趣小组的同学为探究二氧化硫的化学性质,设计了如图所示的装置.请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| x | 温度 | 压强 | SO2的浓度 | 加入催化剂 |
| y | 容器内气体密度 | CO2的体积分数 | 平衡常数 | CO的转化率 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a1、a2均减小 | B. | a1减小,a2增大 | C. | a1、不变,a2增大 | D. | a1不变,a2减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该条件下Z是气态 | B. | 平衡常数K=$\frac{c(Z)•c(W)}{c(X)•c(Y)}$ | ||
| C. | 增加Z平衡逆向移动 | D. | 上述过程中X的转化率变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大反应物的浓度,平衡常数K增大 | B. | 加大体系压强,平衡常数K增大 | ||
| C. | 加入负催化剂,平衡常数K减小 | D. | 升高温度,平衡常数K发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 很多城市对废旧电池进行回收处理 | |
| B. | 有些国家对聚乙烯等塑料垃圾进行了深埋或者倾倒入大海处理 | |
| C. | 不少地区正在使用沼气,太阳能,风能等能源替代传统的煤炭 | |
| D. | 许多地方政府出台相关法规来保护生物物种多样性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
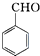 +KOH→
+KOH→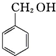 +
+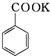
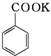 +HCl→
+HCl→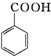 +KCl
+KCl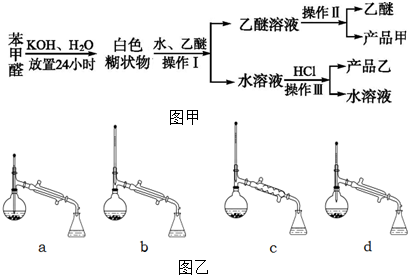
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
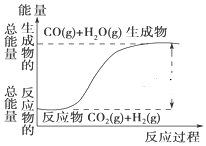
| A. | 其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g)△H=41kJ•mol-1 | |
| B. | 该反应为吸热反应 | |
| C. | 该反应为放热反应 | |
| D. | 当H2O为液态时,其反应热值大于41kJ•mol-1. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com