
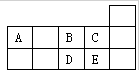
 如表为元素周期表短周期的一部分.下列有关A、B、C、D、E五种元素的叙述中,不正确的是( )
如表为元素周期表短周期的一部分.下列有关A、B、C、D、E五种元素的叙述中,不正确的是( )| A、A与B形成的阴离子可能有:AB32-、A2B42- |
| B、E的氢化物的沸点比C的氢化物的沸点低 |
| C、D在过量的B中燃烧的主要产物为DB3 |
| D、这5种元素形成只含极性键的非极性分子多于4种 |


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:
| A、降低温度 | B、增大压力 |
| C、加入氧气 | D、去掉三氧化硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液肯定显碱性 |
| B、该溶液肯定显酸性 |
| C、该溶液的pH可能是11,也可能是3 |
| D、该溶液的pH肯定不是11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、V(H2)=0.1 mol?Lˉ1?minˉ1 |
| B、V(N2)=0.1 mol?Lˉ1?minˉ1 |
| C、V(NH3)=0.15 mol?Lˉ1?minˉ1 |
| D、V(N2)=0.002 mol?Lˉ1?sˉ1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解熔融CeO2制Ce,铈在阳极获得 | ||||||||
| B、铈溶于氢碘酸的化学方程式可表示为:Ce+4HI═CeI4+2H2↑ | ||||||||
| C、用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+ | ||||||||
D、四种稳定的核素
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 2008年北京奥运会主体育场的外形好似“鸟巢”(The Bird Nest).有一类硼烷也好似鸟巢,故称为巢式硼烷.巢式硼烷除B10H14不与水反应外,其余均易与水反应生成氢气和硼酸,硼烷易被氧化.如图是三种巢式硼烷,有关说法正确的是( )
2008年北京奥运会主体育场的外形好似“鸟巢”(The Bird Nest).有一类硼烷也好似鸟巢,故称为巢式硼烷.巢式硼烷除B10H14不与水反应外,其余均易与水反应生成氢气和硼酸,硼烷易被氧化.如图是三种巢式硼烷,有关说法正确的是( )| A、这类巢式硼烷的通式是BnHn+4 | ||||
B、2B5H9+12O2
| ||||
| C、8个硼原子的巢式硼烷化学式应为B8H10 | ||||
| D、硼烷与水反应是非氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
16 8 |
18 8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
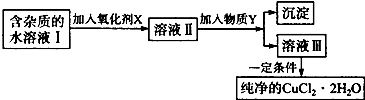
| Fe3+ | Fe+ | Cu+ | |
| 氢氧化物开始沉淀时p | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时p | 3.2 | 9.0 | 6.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com