
【题目】如图是部分短周期元素原子半径与原子序数的关系图。则下列说法不正确的是( )
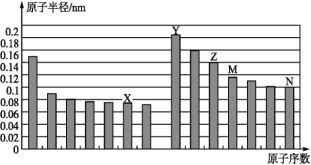
A.Z、N两种元素的离子半径相比,后者较大
B.X、N两种元素的气态氢化物的稳定性相比,前者较强
C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D.Z的氢氧化物能分别溶解于Y的氢氧化物的水溶液和N的氢化物的水溶液
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】元素 R、X、T、Z、Q 在元素周期表中的相对位置如图所示,其中 R 的氢化物的水溶液可以用来刻蚀玻璃,则下列判断正确的是( )
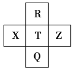
A.气态氢化物的酸性:R>T>Q
B.气态氢化物的还原性:X>T
C.R 与 Q 的电子数相差 16
D.R 的单质通入 T 的钠盐溶液中能置换出T 的单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某食用香料乙酸橙花酯的结构简式如图所示,则关于该有机物叙述中正确的个数是( )

①分子式为C12H20O2 ②它的同分异构体中有芳香族化合物 ③能使酸性KMnO4溶液褪色 ④1mol该有机物在一定条件下能和3mol H2反应 ⑤密度比水小 ⑥1mol该有机物水解时能消耗1molNaOH⑦能在一定条件下生成高分子化合物
A. 3个 B. 4个 C. 5个 D. 6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国成功研制出了具有自主知识产权的治疗缺血性脑梗死新药——丁苯酞。有机物G是合成丁苯酞的中间产物,G的一种合成路线如下:

已知:
回答下列问题:
(1)A的结构简式是___________,E的化学名称是____________。
(2)由B生成C的化学方程式为______________________。
(3)G的结构简式为__________________。合成丁苯酞的最后一步转化为:
 ,则该转化的反应类型是_______________。
,则该转化的反应类型是_______________。
(4)有机物D的溴原子被羟基取代后的产物J有多种同分异构体,其中含有苯环的同分异构体有______种(不包括J),其核磁共振氢谱吸收峰最多的结构简式为_________。
(5)参照题中信息和所学知识,写出用![]() 和CH3MgBr为原料(其他无机试剂任选)制备
和CH3MgBr为原料(其他无机试剂任选)制备![]() 的合成路线:______________。
的合成路线:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1942 年,我国化工专家侯德榜以 NaCl、NH3、CO2 等为原料先制得 NaHCO3,进而生产出纯碱, 他的“侯氏制碱法”为世界制碱工业做出了突出贡献。有关反应的化学方程式如下:
NH3+CO2+H2O=NH4HCO3 ;
NH4HCO3+NaCl=NaHCO3↓+NH4Cl ;
2NaHCO3![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(1)“侯氏制碱法”把合成氨和纯碱两种产品联合生产,请写出工业合成氨的化学反应方程式_______
(2)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是_______。
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(3)某探究活动小组根据上述制碱原理,欲制备碳酸氢钠,同学们按各自设计的方案进行实验。
第一位同学:将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示(图中夹持、固定用的仪器未画出)。
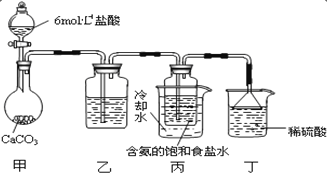
请回答:
①写出甲中发生反应的离子方程式_______。
②乙装置中的试剂是_______。
③实验结束后,分离出 NaHCO3 晶体的操作是_______ (填分离操作的名称)。
第二位同学:用如图装置进行实验(其它装置未画出)。
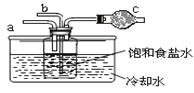
①为提高二氧化碳在此反应溶液中被吸收的程度,实验时,须先从 a 管通入_______气体,再从b 管中通入_______气体。
②装置 c 中的试剂为_______(选填字母)。
e.碱石灰 f..浓硫酸 g.无水氯化钙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[3,3]庚烷(![]() )是其中的一种。下列关于该化合物的说法不正确的是
)是其中的一种。下列关于该化合物的说法不正确的是
A. 与环庚烯互为同分异构体 B. 二氯代物共有6种(不含立体异构)
C. 所有碳原子不可能处在同一平面 D. 1mol该化合物含有20mol共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2﹣环氧丁烷如图,通常为无色液体,用于制造泡沫塑料、合成橡胶、非离子型表面活性剂等。下列关于1,2﹣环氧丁烷的说法不正确的是( )
![]()
A. 化学式为C4H8O
B. 氧原子与所有碳原子可能处于同一平面
C. 能发生氧化反应和取代反应
D. 二溴代物的结构有9种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
①增加C的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大 ④保持压强不变,充入N2使容器体积变大
A.①④B.②③C.①③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有 A、B、C、D、E 五种短周期元素,已知 A、B、C、D 四种元素的核内质子数 之和为 56,在元素周期表中的位置如图所示,1 mol E 的单质可与足量酸反应,能产生 33.6 L H2(在标准状况下);E 的阳离子与 A 的阴离子核外电子层结构相同。回答下列问题:

(1)写出下列元素名称 A_______,B_______, E_______
(2)C 的简单离子结构示意图为_______
(3)A 与 E 形成的化合物的化学式为_______,它的性质决定了它在物质的分类中应属于_______
(4)D 和 E 形成化合物在熔融状态下不导电,原因是______。
(5)向 D 与 E 形成的化合物的水溶液中滴入烧碱溶液至过量,此过程中观察到的现象是______,写出有关化学反应方程式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com