
| A. | Fe2O3 | B. | NaCl | C. | Cu2S | D. | Al2O3 |
分析 电解法:冶炼活泼金属K、Ca、Na、Mg、Al,一般用电解熔融的氯化物(Al是电解熔融的Al2O3)制得;
热还原法:冶炼较不活泼的金属Zn、Fe、Sn、Pb、Cu,常用还原剂有(C、CO、H2等);
热分解法:冶炼不活泼的金属Hg、Ag用加热分解氧化物的方法制得.
解答 解:A.Fe用热还原法冶炼,故A不选;
B.钠的性质很活泼,用电解氯化钠的方法冶炼,故B选;
C.Cu用热还原法冶炼,故C不选;
D.Al的性质很活泼,用电解其氧化物的方法冶炼,故D选.
故选BD.
点评 本题考查金属冶炼的一般方法和原理,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,注意根据金属的活泼性采用相应的冶炼方法,难度不大.


科目:高中化学 来源: 题型:解答题
| 实验组 | 温度℃ | 超始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO2 | |||
| 1 | 650 | 4 | 2 | 1.6 | 1.6 | 5 |
| 2 | 900 | 2 | 1 | 0.5 | 0.5 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C60气化和I2升华克服的作用力相同 | |
| B. | 高温结构陶瓷材料Si3N4固体是分子晶体 | |
| C. | 分子晶体在水溶液中一定导电 | |
| D. | NaCl和HCl溶于水时,均破坏都是离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 HClO+OH-.
HClO+OH-.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
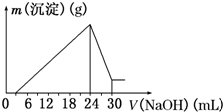 铝是现今人类生产生活中使用广泛性仅次于铁的重要金属.工业上常以“钒土矿”为原料来冶炼金属铝.已知:钒土的主要成分是Al2O3(其中含有Fe2O3、SiO2等杂质).为了检测某“钒土矿”样中Al2O3的含量,进行了如下实验过程:
铝是现今人类生产生活中使用广泛性仅次于铁的重要金属.工业上常以“钒土矿”为原料来冶炼金属铝.已知:钒土的主要成分是Al2O3(其中含有Fe2O3、SiO2等杂质).为了检测某“钒土矿”样中Al2O3的含量,进行了如下实验过程:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 其反应的装置示意图如图1(夹持装置、加热装置略去):环己醇、环己酮、饱和食盐水和水的部分物理性质见下表:
其反应的装置示意图如图1(夹持装置、加热装置略去):环己醇、环己酮、饱和食盐水和水的部分物理性质见下表:| 物质 | 沸点(℃) | 密度(g•cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8) | 0.9624 | 能溶于水 |
| 环己酮 | 155.6(95) | 0.9478 | 微溶于水 |
| 饱和食盐水 | 108.0 | 1.3301 | |
| 水 | 100.0 | 0.9982 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com