
| A. | 过氧化钠与二氧化硫反应时可生成硫酸钠 | |
| B. | 1mol过氧化钠中阴离子数目约为6.02×1023 | |
| C. | Na2O2与CO2反应时,Na2O2是氧化剂CO2是还原剂 | |
| D. | 将等物质的量的Na2O和Na2O2分别溶于等质量的足量水中所得溶液的质量相等 |
分析 过氧化钠电子式为: ,是由2个钠离子与1个过氧根离子通过离子键结合而成的离子化合物,具有强氧化性,可与木炭、铝粉以及二氧化硫等反应,以此解答该题.
,是由2个钠离子与1个过氧根离子通过离子键结合而成的离子化合物,具有强氧化性,可与木炭、铝粉以及二氧化硫等反应,以此解答该题.
解答 解:A.过氧化钠具有强氧化性,与二氧化硫反应生成硫酸钠,没有氧气生成,故A正确;
B.氧化钠电子式为: ,1mol过氧化钠中阴离子数目为6.02×1023,故B正确;
,1mol过氧化钠中阴离子数目为6.02×1023,故B正确;
C.过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应中过氧化钠既是氧化剂也是还原剂,故C错误;
D.根据反应方程式:Na2O+H2O=2NaOH①,2Na2O2+2H2O=4NaOH+O2↑②,可知①②式中等物质的量的Na2O、Na2O2消耗H2O一样多,产生溶质NaOH一样多,则所得溶液的质量相等,故D正确.
故选C.
点评 本题考查了过氧化钠性质的应用分析,为高频考点,侧重于过氧化钠氧化性的考查,注意把握题给信息以及过氧化钠的构成特点,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
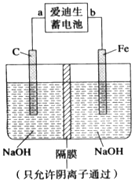 铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:
铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 425mL | B. | 560mL | C. | 250mL | D. | 500mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锂离子电池充电时电池反应为C6Li+Li1-xMO2═LiMO2+C6Li1-x | |
| B. | 电池反应中,锂、锌、银、铅各失去1mol电子,金属锌所消耗的质量最小 | |
| C. | 锂离子电池放电时电池内部Li+向负极移动 | |
| D. | 锂离子电池充电时阴极反应为C6Li1-x+xLi++x e-═C6Li |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②④ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤⑥ | B. | ①③⑤ | C. | ①②③⑤⑥ | D. | ①③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
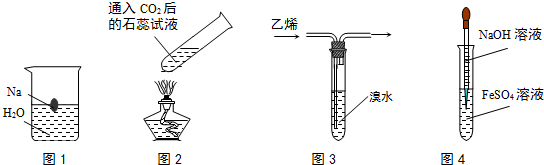
| A. | 图1中溶液颜色变化:无色→红色 | |
| B. | 图2中溶液颜色变化:红色→紫色 | |
| C. | 图3中溴水颜色变化:红棕色→无色 | |
| D. | 图4中生成的沉淀颜色变化:白色→绿色→红褐色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将搪瓷快餐杯脱瓷的部位用醇酸油漆涂严实,防止杯被腐蚀 | |
| B. | 将自行车的铁链条涂上植物油,防止链条被腐蚀 | |
| C. | 将埋在地下的铜水管缠上废铁丝,防止水管被腐蚀 | |
| D. | 将待埋在地下的木头桩先用火将表面烧焦,防止木材被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含分子数相同 | B. | 质量之比为16:17 | ||
| C. | 所含氢原子的物质的量之比为3:4 | D. | 密度之比为17:16 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com