
【题目】常用作风信子等香精的定香剂D以及可用作安全玻璃夹层的高分子化合物PVB的合成路线如下:

已知:Ⅰ.RCHO+R’CH2CHO![]()
![]() +H2O(R、R’表示烃基或氢)
+H2O(R、R’表示烃基或氢)
Ⅱ.醛与二元醇![]() 如:乙二醇
如:乙二醇![]() 可生成环状缩醛:RCHO+HOCH2CH2OH
可生成环状缩醛:RCHO+HOCH2CH2OH![]()
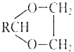 +H2O
+H2O
⑴A的核磁共振氢谱有两种峰.A的名称是 ______
⑵下列关于B的说法正确的是 ______
a.分子式为C9H8O b.所有原子均可在同一平面上
c.最多可以与5molH2发生反应 d.可以使溴水褪色
⑶C为反式结构,由B还原得到。C的结构简式是 ______
⑷G与D含有相同的官能团,相对分子量比D小28,则G的结构有 ______ 种![]() 不包括立体异构
不包括立体异构![]()
⑸E能使Br2的CCl4溶液褪色,N由A经反应①③合成。
a.②的反应类型是 ______
b.③的化学方程式是 ______
⑹PVAc由一种单体经加聚反应得到,该单体的结构简式是 ______
⑺碱性条件下,PVAc完全水解的化学方程式是 ______
【答案】乙醛 abcd ![]() 6 加成反应 2CH3(CH2)3OH+O2
6 加成反应 2CH3(CH2)3OH+O2 ![]() 2CH3(CH2)2CHO+2H2O CH3COOCH=CH2
2CH3(CH2)2CHO+2H2O CH3COOCH=CH2 ![]() +nNaOH
+nNaOH![]()
![]() +nCH3COONa
+nCH3COONa
【解析】
根据A的分子式和A转化为B的反应条件,结合题给信息I和A的核磁共振氢谱,可以确定A为乙醛,B为![]() ;由C为反式结构,由B还原得到,可以确定C中仍具有C=C,被还原的基团应是-CHO,由此即可确定C的结构式
;由C为反式结构,由B还原得到,可以确定C中仍具有C=C,被还原的基团应是-CHO,由此即可确定C的结构式![]() ;根据D的分子式C11H12O2,可以确定其不饱和度为6,结合生成D的反应条件,可确定D为
;根据D的分子式C11H12O2,可以确定其不饱和度为6,结合生成D的反应条件,可确定D为![]() ,进而确定M为乙酸;由PVB的结构简式和题给信息II可确定其单体之一是CH3(CH2)2CHO,即N为CH3(CH2)2CHO;另一高分子化合物PVA为
,进而确定M为乙酸;由PVB的结构简式和题给信息II可确定其单体之一是CH3(CH2)2CHO,即N为CH3(CH2)2CHO;另一高分子化合物PVA为![]() ,进而推出PVAc的单体为CH3COOCH=CH2;由A和N的结构简式,结合题给信息I即可推出E为CH3CH=CHCHO,F为CH3(CH2)3OH。
,进而推出PVAc的单体为CH3COOCH=CH2;由A和N的结构简式,结合题给信息I即可推出E为CH3CH=CHCHO,F为CH3(CH2)3OH。
⑴A的分子式是C2H4O,且A的核磁共振氢谱有两种峰,因此A只能是乙醛;
⑵B为![]() ,
,
a.B的分子式为C9H8O,故a正确;
b.苯环上、碳碳双键上及碳氧双键上所有原子共面,单键可以转动,所以B的所有原子均可在同一平面上,故b正确;
c.B中有一个苯环、一个碳碳双键、一个碳氧双键,所以最多可以与5molH2发生反应,故c正确;
d.B中有碳碳双键,可以使溴水褪色,故d正确;
故选abcd;
⑶C为反式结构,说明C中含有碳碳双键.又因为C由B还原得到,B中含有醛基,因此C中含有羟基,故C的结构简式是![]() ;
;
⑷D为![]() ,G与D含有相同的官能团,即含有酯基和碳碳双键,相对分子量比D小28,即少两个碳和四个氢,则G的结构为苯环上连有-CH=CHOOCH,或-COOCH=CH2,或-OOCCH=CH2,或连有-CH=CH2、-OOCH,这样的结构有邻间对三种,所以共有6种;
,G与D含有相同的官能团,即含有酯基和碳碳双键,相对分子量比D小28,即少两个碳和四个氢,则G的结构为苯环上连有-CH=CHOOCH,或-COOCH=CH2,或-OOCCH=CH2,或连有-CH=CH2、-OOCH,这样的结构有邻间对三种,所以共有6种;
⑸根据PVB的结构简式并结合信息Ⅱ可推出N的结构简式是CH3(CH2)2CHO,又因为E能使Br2的CCl4溶液褪色,所以E是2分子乙醛在氢氧化钠溶液中并加热的条件下生成的,即E的结构简式是CH3CH=CHCHO,然后E通过氢气加成得到F,所以F的结构简式是CH3(CH2)3OH,F经过催化氧化得到N,方程式为2CH3(CH2)3OH+O2 ![]() 2CH3(CH2)2CHO+2H2O;
2CH3(CH2)2CHO+2H2O;
⑹根据上面的分析可知,PVAc的单体为CH3COOCH=CH2;
⑺PVAc为![]() ,含有酯基,能在碱性条件下水解生成
,含有酯基,能在碱性条件下水解生成![]() 和乙酸钠,反应的化学方程式为
和乙酸钠,反应的化学方程式为![]() +nNaOH
+nNaOH![]()
![]() +nCH3COONa。
+nCH3COONa。


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:
【题目】甲醇来源丰富,有广泛的用途和广阔的应用前景,工业上可以利用CO和CO2生产甲醇,同时可以利用甲醇生产丙烯。制备甲醇,丙烯过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.0kJ/mol
CH3OH(g)+H2O(g) △H1=-49.0kJ/mol
反应Ⅱ:CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g)![]() CH3OH(g) △H3=-90.0kJ/mol
CH3OH(g) △H3=-90.0kJ/mol
反应Ⅳ:3CH3OH(g)![]() C3H6(g)+3H2O(g) △H4=-31.0kJ/mol
C3H6(g)+3H2O(g) △H4=-31.0kJ/mol
回答下列问题:
(1)反应Ⅱ的ΔH2=________。
(2)反应Ⅲ能够自发进行的条件是________(填“较低温度”“较高温度”或“任何温度”),据研究该反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于保持催化剂Cu2O的量不变,原因是________(用化学方程式表示)。
(3)恒温,恒容密闭容器中,对于反应Ⅰ,下列说法中能说明该反应达到化学平衡状态的是________。
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2的生成速率与CH3OH的生成速率相等
D.容器的压强不再变化
(4)甲醇生产丙烯的同时,还生成乙烯。在某催化剂作用下,2L密闭容器中加入0.5mol甲醇,经过相同时间后测得甲醇转化率及丙烯的选择性(生成丙烯的甲醇与甲醇转化量的比值)与反应温度之间的关系如图所示。计算600℃时反应甲醇生产丙烯的反应Ⅳ平衡常数________。若将容器体积压缩为1L,其他条件不变,在如图中作出甲醇平衡转化率随温度的变化曲线。________。
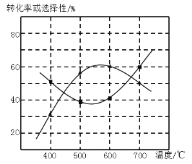
(5)研究表明,甲醇可由CO2在强酸性水溶液中通过电解合成,则生成甲醇的反应电极反应式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 | 实验结论 |
(1)称取A4.5g,升温使其汽化,测其密度是相同条件下H2的45倍。 | (1)A的相对分子质量为:___。 |
(2)将此4.5g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6g。 | (2)A的分子式为:____。 |
(3)另取A 4.5g,跟足量的NaHCO3粉末反应,生成1.12L CO2(标准状况),若与足量金属钠反应则生成1.12L H2(标准状况)。 | (3)写出A中含有的官能团(用结构简式表示)____。 |
(4)A的核磁共振氢谱如图: | (4)综上所述,A的结构简式为________。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A.σ键比π键的电子云重叠程度大,形成的共价键强
B.s-sσ键与s-pσ键的电子云形状对称性相同
C.丙烯(CH3—CH=CH2)分子有8个σ键,1个π键,其中碳原子分别是sp2、sp3杂化
D.N2分子中有一个σ键,2个π键;NH4+中4个N-H键的键能不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个电化学过程的示意图,请按要求填空:

(1)通入CH3CH2OH的电极名称是______________,B电极的名称是_____________。
(2)通入CH3CH2OH一极的电极反应式为_____________________________________。
(3)乙池中总反应的化学方程式为___________________________________________。
(4)当乙池中A(Fe)极的质量增加12.8g时,甲池中消耗O2 _______ mL(标况下)
(5)火箭发射时可用肼(N2H4)为燃料,以二氧化氮做氧化剂,它们相互反应生成氮气和水蒸气。
①写出在碱性条件下负极反应式为:___________________________________________。
②已知:N2(g)+2O2(g)=2NO2(g),ΔH=+67.7 kJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g),ΔH=-534 kJ·mol-1,则N2H4和NO2反应的热化学方程式__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为![]() 的有机物A有下列变化:
的有机物A有下列变化:

其中B、C的相对分子质量相等,下列有关说法错误的是( )
A.C和E互为同系物
B.符合题目条件的A共有4种
C.D既能发生氧化反应,又能发生还原反应
D.符合题目条件的B共有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 | 实验结论 |
(1)称取A4.5g,升温使其汽化,测其密度是相同条件下H2的45倍。 | A的相对分子质量为:___。 |
(2)将此4.5gA在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6g。 | A的分子式为:___。 |
(3)另取A4.5g,跟足量的NaHCO3粉末反应,生成1.12LCO2(标准状况),若与足量金属钠反应则生成1.12LH2(标准状况)。 | 写出A中含有的官能团___、__。 |
(4)A的核磁共振氢谱如图: | 综上所述,A的结构简式为___。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前生产聚氯乙烯的方法是先使乙烯与氯气和氧气在一定条件下反应生成氯乙烯和水,再进一步合成聚氯乙烯。请回答
(1)请写出上述两个过程所发生反应的化学方程式:①____________________________,②__________________________________________。
(2)聚氯乙烯是一种可燃物,火灾中聚氯乙烯燃烧会产生有害气体,其主要成分可能是_________;若在火灾现场,为了防止气体中毒,应采取的防护措施是__________________________________________。
(3)聚氯乙烯___________(填“可以”或“不可以”)用于制作食品包装袋,原因是______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟在自然界中常以CaF2的形式存在。
(1)下列关于CaF2的表述正确的是________。
a.Ca2+与F-间仅存在静电吸引作用
b.F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2
c.阴阳离子比为2∶1的物质,均与CaF2晶体构型相同
d.CaF2中的化学键为离子键,因此CaF2在熔融状态下能导电
(2)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是_______________(用离子方程式表示)。已知AlF![]() 在溶液中可稳定存在。
在溶液中可稳定存在。
(3)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为________,其中氧原子的杂化方式为________。
(4)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)===2ClF3(g) ΔH=-313 kJ·mol-1,F—F键的键能为159 kJ·mol-1,Cl—Cl键的键能为242 kJ·mol-1,则ClF3中Cl—F键的平均键能为________kJ·mol-1。ClF3的熔、沸点比BrF3的________(填“高”或“低”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com