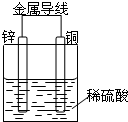
������һ�������£�������Ӧ��
aA��g��+bB��g��?cC��g����H=Q kJ/mol���仯ѧƽ�ⳣ��K���¶ȵĹ�ϵ���±���ʾ��
| t�� |
400 |
500 |
800 |
1000 |
| K |
2.6 |
1.6 |
1.0 |
0.40 |
����ͼ���жϸ÷�Ӧ��H
0�����������������������������һ���������¶ȣ��÷�Ӧ��A��ת����
�����������С�����䡱��ͬ������ѧ��Ӧ���ʽ�
��
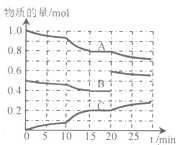
�����ں㶨�¶�t�棬2L�����ܱ������з�����ӦaA��g��+bB��g��?cC��g����������A��B��C���ʵ����仯��ͼ��ʾ���ش��������⣺
��1���û�ѧ����ʽ��a��b��cΪ
��t��ʱ�÷�Ӧ�Ļ�ѧƽ�ⳣ��K��ֵΪ
��������2λС����
��2��0��15min�ڣ�B��ƽ����Ӧ����Ϊ
����Ӧ��ƽ��ʱ��A��ת����Ϊ
��
��3����ͼ�жϣ���Ӧ������20minʱ�����߷����仯��ԭ����
�������ֱ������Ӧ���´�ƽ��ʱ��A�����������
�����������С�����䡱����
��4��10min��15min�����߱仯��ԭ�������
��

 ������һ�������£�������Ӧ��
������һ�������£�������Ӧ��