
| 序号 | 反应温度/℃ | C(H2O2)/mol-L | V(H2O2)/mL | M(MnO2)/g | t/min |
| 1 | 20 | 2 | 10 | 0 | t1 |
| 2 | 20 | 2 | 10 | 0.1 | t2 |
| 3 | 20 | 4 | 10 | 0.1 | t3 |
| 4 | 40 | 2 | 10 | 0.1 | t4 |
分析 (1)实验2和实验3是双氧水的浓度不同;
(2)实验2和实验4其他条件都相同,只有温度不同;
(3)试验1和实验2相比较,2中使用了催化剂,其他条件相同.
解答 解:(1)实验2和实验3是双氧水的浓度不同,则实验目的为研究双氧水浓度不同,对化学反应速率的影响,
故答案为:H2O2的浓度;
(2)实验2和实验4其他条件都相同,只有温度不同,这两个实验是研究温度对化学反应速率的影响,
故答案为:2;4;
(3)试验1和实验2相比较,2中使用了催化剂,其他条件相同,反应速率大,所用时间短,
故答案为:>.
点评 本题考查了影响化学反应速率的因素的探究,注意熟练掌握影响化学反应速率的因素,利用控制变量法是解本题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 4-甲基-3-丙基戊烷 | B. | 3-异丙基己烷 | ||
| C. | 2-甲基-3-丙基戊烷 | D. | 2-甲基-3-乙基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 现象 | 结论 | |
| A | 室温下测0.1mol•L-1醋酸pH | pH≈3.3 | 醋酸是弱酸 |
| B | 向2mL 0.1mol•L-1NaOH溶液中 i.滴加几滴同浓度的MgSO4溶液 ii.再滴加几滴同浓度FeCl3溶液 | i.产生白色沉淀 ii.产生红褐色沉淀 | 溶解度:Fe(OH)3<Mg(OH)2 |
| C | 常温下,将CO2通入苯酚钠溶液中 | 溶液变浑浊 | 酸性:碳酸>苯酚 |
| D | 将少量溴乙烷与NaOH溶液共热,冷却、HNO3酸化后,滴加AgNO3溶液 | 淡黄色沉淀 | 证明含有溴元素 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. →
→ ,元素⑥和⑨形成的化合物中含有离子键.
,元素⑥和⑨形成的化合物中含有离子键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | B的物质的量浓度 | D. | 混合气体的平均相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成物化学键形成时也会吸收热量 | |
| B. | 生成物的总能量高于反应物的总能量 | |
| C. | 一定需要加热条件下才能实现 | |
| D. | 使用催化剂可以降低吸热反应的热效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
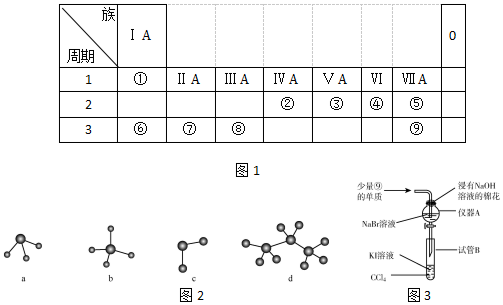
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ① | ⑦ | ④ | ||||
| 3 | ③ | ⑤ | ⑧ | ⑩ | ||||
| 4 | ② | ⑨ |
 ;
; .
.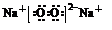 ;④⑧⑨元素的离子的还原性由强到弱顺序为Br->Cl->F-(用离子符号).
;④⑧⑨元素的离子的还原性由强到弱顺序为Br->Cl->F-(用离子符号).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com