
分析 ①E的原子核中含有20个中子,1.11g ECl2与20mL 1mol•L-1的AgNO3溶液恰好完全反应生成AgCl沉淀,说明1.11g ECl2物质的量为0.01mol,即$\frac{1.11g}{(M+35.5×2)g/mol}$=0.01mol,得M=40,所以E为Ca元素;
②B的单质可与酸反应,1molB单质与足量酸作用,在标准状况下能产生33.6L H2,即1molB反应失去3mol电子,B在盐中的化合价为+3价,所以B为Al元素;
③C单质在标准状况下的密度为3.17g/L,则标准状况下1molC单质体积为22.4L,质量m=3.17g/L×22.4L,摩尔质量M=$\frac{m}{n}$=71g/L,所以C为Cl元素;
A、B、C、D、E为五种常见的元素,原子序数逐渐增大,A、E同主族,A为Mg元素;
D、E同周期,D为K元素,由此解答.
解答 解:①E的原子核中含有20个中子,1.11g ECl2与20mL 1mol•L-1的AgNO3溶液恰好完全反应生成AgCl沉淀,说明1.11g ECl2物质的量为0.01mol,即$\frac{1.11g}{(M+35.5×2)g/mol}$=0.01mol,得M=40,所以E为Ca元素;
②B的单质可与酸反应,1molB单质与足量酸作用,在标准状况下能产生33.6L H2,即1molB反应失去3mol电子,B在盐中的化合价为+3价,所以B为Al元素;
③C单质在标准状况下的密度为3.17g/L,则标准状况下1molC单质体积为22.4L,质量m=3.17g/L×22.4L,摩尔质量M=$\frac{m}{n}$=71g/L,所以C为Cl元素;
A、B、C、D、E为五种常见的元素,原子序数逐渐增大,A、E同主族,A为Mg元素;
D、E同周期,D为K元素,
(1)Al单质与K的最高价氧化物对应水化物(KOH)反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2;
(2)A、E最高价氧化物对应水化物分别为Ca(OH)2和Mg(OH)2,元素金属性越强对应最高价氧化物对应水化物碱性越强,所以其碱性强弱顺序为Ca(OH)2>Mg(OH)2,故答案为:Ca(OH)2>Mg(OH)2;
(3)Ca为活泼金属,能与水反应生成碱和水,其化学方程式为Ca+2H2O=Ca(OH)2+H2,故答案为:Ca+2H2O=Ca(OH)2+H2;
(4)实验室制取Cl单质是利用二氧化锰和浓盐酸反应制取,其离子反应方程式为MnO2+4H++2Cl-=Mn2++Cl2+2H2O,故答案为:MnO2+4H++2Cl-=Mn2++Cl2+2H2O.
点评 本题考查位置结构与性质的关系及元素周期表和元素周期律,为高频考点,把握元素的位置分析元素为解答的关键,注重基础知识的考查,题目难度不大.


科目:高中化学 来源: 题型:填空题
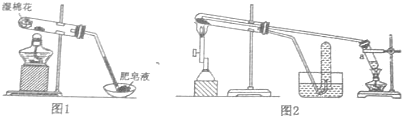
| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 将反应后得到的黑色固体X,取出少量放人另一试管中,加人少量盐酸,微热 | 黑色粉末逐渐溶解,产生少量气泡 |
| Ⅱ | 向上述实验得到的溶液中滴加几滴KSCN溶液,振荡 | 溶液未出现红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
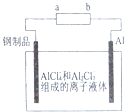 已知:银锌电池放电时总反应为Zn+Ag2O+H2O═Zn(OH)2+2Ag,用银锌电池作电源,在非水体系中完成钢制品上镀铝的原理如图所示,下列说法正确的是( )
已知:银锌电池放电时总反应为Zn+Ag2O+H2O═Zn(OH)2+2Ag,用银锌电池作电源,在非水体系中完成钢制品上镀铝的原理如图所示,下列说法正确的是( )| A. | a电极的电极反应式为Ag2O+H2O+2e-=2Ag+2OH- | |
| B. | 银锌电池的电解质溶液可用稀硫酸 | |
| C. | 银锌电池放电时,负极附近溶液的pH增大 | |
| D. | Al电极上发生的电极反应式为Al+7AlCl4--3e-=4Al2Cl4- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第一主族的元素称为碱金属 | |
| B. | 第二周期元素的最高化合价依次递增,并等于它所处的主族序数 | |
| C. | 短周期元素形成离子后,最外层电子都达到8电子稳定结构 | |
| D. | 同一主族的元素的原子,最外层电子数一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
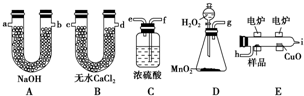
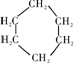 .若该有机物M能使溴水褪色,且所有碳原子共面,则M的结构简式为(CH3)2C=C(CH3)2.
.若该有机物M能使溴水褪色,且所有碳原子共面,则M的结构简式为(CH3)2C=C(CH3)2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 | |
| 2 | ① | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | |||||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知NaHA溶液呈碱性,则该溶液中:c(A2-)>c(H2A) | |
| B. | 在小苏打溶液中存在下列关系:c(HCO3-)+c (CO32-)=c(Na+) | |
| C. | 常温下,稀释0.1 mol/L的氨水,水的电离程度减小 | |
| D. | 向AgCl悬浊液中加入足量的NaI,会观察到有黄色沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com