
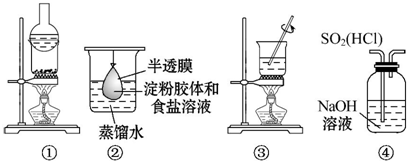
| A. | 用①分离氯化铵和单质碘 | |
| B. | 用②除去淀粉溶液中的氯化钠 | |
| C. | 用③加热胆矾(CuSO4•5H2O)制取无水硫酸铜 | |
| D. | 用④装置除去SO2中的HCl |
分析 A.加热时碘升华,氯化铵分解,温度稍低又变为固体;
B.胶体不能透过半透膜;
C.加热固体应在坩埚中;
D.二者都与氢氧化钠溶液反应.
解答 解:A.加热时碘升华,氯化铵分解,温度稍低又变为氯化铵固体,不能分离二者,故A错误;
B.胶体不能透过半透膜,可用渗析的方法分离,故B正确;
C.加热固体应在坩埚中,不能用烧杯,防止温度过高而导致炸裂,故C错误;
D.二者都与氢氧化钠溶液反应,应用饱和亚硫酸氢钠溶液除杂,故D错误.
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质的分离、制备等,把握实验原理及实验装置图的作用为解答的关键,注意方案的合理性、操作性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ClO2具有强还原性,可用于自来水的杀菌消毒 | |
| B. | 晶体硅具有导电性,可用于制作光导纤维 | |
| C. | MgO的熔点很高,可用于制作耐高温材料 | |
| D. | 浓硫酸具有吸水性,可用于干燥氯气、氨气等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li是负极,电极反应为Li-e-═Li+ | |
| B. | 锂电池属于一次性电池 | |
| C. | MnO2是正极,电极反应为MnO2+e-═MnO${\;}_{2}^{-}$ | |
| D. | 锂电池是一种环保型电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
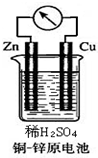 如图所示的铜-锌原电池中,理论上应观察到的现象是:
如图所示的铜-锌原电池中,理论上应观察到的现象是:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
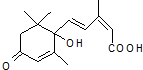 农艺师对盆栽施用S-诱抗素剂(分子结构如图),可以使鲜花按时盛开.下列说法不正确的是( )
农艺师对盆栽施用S-诱抗素剂(分子结构如图),可以使鲜花按时盛开.下列说法不正确的是( )| A. | S-诱抗素的分子式为C15 H20 O4 | |
| B. | S-诱抗素既能发生加聚反应,又能发生缩聚反应 | |
| C. | 1 mol S-诱抗素最多能和含1 mol NaOH的水溶液发生反应 | |
| D. | S-诱抗素既可以与FeCl3溶液发生显色反应,又可以使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 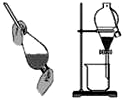 如图装置可用于分离甲苯和液溴的混合物 | |
| B. | 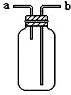 如图装置可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 | |
| C. | 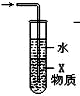 如图装置中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 | |
| D. | 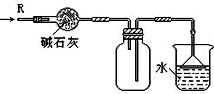 如图装置可用于干燥、收集NH3,并吸收多余的NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 如图是一次性电池--铜锌电池的简易装置.
如图是一次性电池--铜锌电池的简易装置.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com