
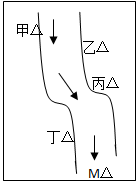
 在一条鱼虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如图所示,箭头表示河水流向),它们排出的废液里,每个工厂只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水检测时发现:①甲处河水呈乳白色,②乙处河水呈红褐色混浊,③丙处河水由浑变清,④丁处产生气泡,河水仍清,⑤M处水样的pH小于7.
在一条鱼虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如图所示,箭头表示河水流向),它们排出的废液里,每个工厂只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水检测时发现:①甲处河水呈乳白色,②乙处河水呈红褐色混浊,③丙处河水由浑变清,④丁处产生气泡,河水仍清,⑤M处水样的pH小于7.分析 水流方向是由甲经过乙,依次流经丙和丁,根据四种物质的性质特点,甲处河水呈乳白色,故为Ca(OH)2;乙处河水呈红褐色是因为生成了Fe(OH)3,故乙处为FeCl3;丙处河水由浑变清,是由于Fe(OH)3沉淀在丙处被溶解,故丙处为盐酸,丁处为Na2CO3(与盐酸作用产生气泡),以此解答该题.
解答 解:(1)由以上分析可知甲为Ca(OH)2,在乙处生成,丙处发生Fe(OH)3+3 H+=Fe3++3H2O,丁处生成的气体为二氧化碳,与氢氧化钡反应的离子方程式为CO2+Ba2++2OH-=BaCO3↓+H2O,
故答案为:Ca(OH)2;Fe(OH)3;Fe(OH)3+3 H+=Fe3++3H2O;CO2+Ba2++2OH-=BaCO3↓+H2O;
(2)丙处为盐酸,丁处为Na2CO3与盐酸作用产生气泡,同时生成氯化钠,则含有的阴离子为Cl-,故答案为:Cl-.由制备实验装置可知,为固体与液体反应制备气体,且不需要加热,气体的密度比空气密度大,为向上排空气法收集,以此来解答.解:饱和食盐水和稀硫酸不反应,不能制备HCl,故A不选;
B.生成硫酸钙微溶,包裹在碳酸钙的表面,阻止反应的发生,故B不选;
C.氢气的密度比空气密度小,应选向下排空气法收集,故C不选;
D.为固体与液体反应生成氧气,且氧气的密度比空气密度大,可利用向上排空气法收集,故D选;
故选D.
点评 本题以四种常见物质之间的离子反应为切入点,从环保的角度考查知识的实际应用,为高频考点,侧重考查学生的分析能力,本题实质是框图型物质推断题,根据物质的溶解性,确定甲处废水含有Ca(OH)2,是推断的突破口,再结合物质间的反应判断.


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②④⑤ | C. | ①④⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.4 g镁在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.8 NA | |
| B. | 标准状况下,5.6 L二氧化碳气体中含有的氧原子数为0.5 NA | |
| C. | 8.7 g MnO2与40 mL 10 mol/L的浓盐酸充分反应,生成的氯气分子数为0.1 NA | |
| D. | 0.1 L 0.5 mol/L CH3COOH溶液中含有的氢离子数为0.05 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 实验步骤 | 预期的现象和结论 |
| ①测定B中实验所用混合溶液的 ②配制具有相同pH的稀硝酸与 BaCl2的混合液并通入适当的N2 ③将SO2通入上述溶液中 | 若出现白色沉淀则假设2成立 若不出现白色沉淀则假设2不成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 第一步需选用仪器①、②和⑨,仪器①的名称叫坩埚 | |
| B. | 第二步用浓硝酸溶解茶叶灰,可能将Fe2+氧化成Fe3+ | |
| C. | 要完成第三步,需选用④、⑤和⑦,除夹持仪器外还缺滤纸 | |
| D. | 第四步,用试剂⑧检验滤液中的Fe3+,溶液中生成血红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在H2SO4溶液中滴入Ba(OH)2溶液至溶液呈中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| C. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ | |
| D. | 醋酸溶解鸡蛋壳:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
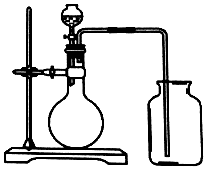
| A. | 锌和稀硫酸 | B. | 碳酸钙和硫酸 | ||
| C. | 过氧化氢和二氧化锰 | D. | 硫酸铵和氢氧化钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24升 | B. | 3.36升 | C. | 4.48升 | D. | 5.6升 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com