
水的电离平衡曲线如图所示,若以A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度,则下列说法正确的是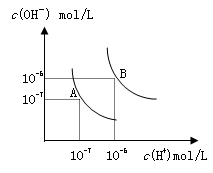
| A.纯水中25℃时的c(H+)比100℃时的c(H+)大 |
| B.100℃时某溶液中由水电离产生的c(H+)=1×10-11mol/L,则该溶液的pH可能是11或3 |
| C.将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 |
| D.25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,则溶液中c(Na+):c(OH-)为104:1 |
D
解析试题分析:A、水的电离为吸热反应,升高温度,水的电离程度增大,氢离子浓度增大,所以纯水中25°C时的c(H+)比100℃的时c(H+)小,错误;B、根据题给图像知,100℃时水的离子积为10-12,由水电离产生的c(H+)=1×10-11mol?L-1,若溶液为酸性溶液,氢离子浓度为:0.1mol/L,溶液的pH=1;若溶液为碱性溶液,则溶液中氢离子浓度为1×10-11mol?L-1,溶液pH=11,错误;C、100℃时水的离子积为10-12,混合溶液的pH=7,反应后的溶液为碱性溶液,溶液中氢离子浓度为1×10-7mol?L-1,氢氧根离子浓度为1×10-5mol?L-1; pH=9的Ba(OH)2溶液中氢氧根离子浓度为1×10-3mol?L-1,与pH=4的稀盐中氢离子浓度为1×10-4mol?L-1,设氢氧化钡的体积为x,盐酸溶液的晶体为y,则:(10?3x?10?4y)/(x+y) =1×10-5,解得x:y=1:10,错误;D、25℃时,氢离子浓度为1.0×10-7mol/L,钠离子浓度为1.0×10-3mol/L,则溶液中c(Na+):c(OH-)=1.0×10-3mol/L:1.0×10-7mol/L=104:1,正确。
考点:考查水的电离、溶液pH的计算。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
在100mL1.0×10-4mol/L的KCl溶液中,加入100mL2.0×10-6mol/L的AgNO3溶液,下列说法正确的是( )
| A.有AgCI沉淀生成 | B.无AgCI沉淀生成 | C.有沉淀生成但不是AgCI | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知室温时,0.1mo1/LCH3COOH在水中有0.1%发生电离,下列叙述正确的是:
| A.该溶液的pH=5 |
| B.由CH3COOH电离出的c(H+)约为水电离出的c(H+)的106倍 |
C.CH3COOH的电离平衡常数约为1×10-6 |
| D.升高温度,溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温时,下列叙述正确的是
| A.pH=9的NH4Cl与NH3?H2O混合溶液中c(Cl-)>c(NH4+) |
| B.pH=2.5的可乐中c(H+) 是pH=3.5的柠檬水中c(H+)的10倍 |
| C.AgCl在0.1mol /L CaCl2溶液和0.1mol/L NaCl溶液中的溶解度相同 |
| D.1 mL 1mol /L Na2CO3溶液加水稀释至100mL, pH和Kw均减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在100mL0.1mol/L醋酸溶液中加入以下物质中的一种,醋酸溶液pH变小。所加入的这种物质是
| A.水 | B.0.1mol/L盐酸 |
| C.醋酸钠晶体 | D.0.1mol/L氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是
| A.c(H+)等于l×l0-7mol/L的溶液一定是中性溶液 |
| B.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其Kw= l×l0-14 |
| C.将水加热,Kw增大,pH不变 |
| D.任何浓度的溶液都可以用pH来表示其酸性的强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列物质的制取,实验操作正确的是
| A.将CuCl2溶液置于蒸发皿中加热蒸干,可制取无水CuCl2固体 |
| B.将NH4HCO3饱和溶液置于蒸发皿中加热蒸于,可制取NH4HCO3固体 |
| C.向FeCl3饱和溶液中缓慢滴入过量氨水加热,可制取Fe(OH)3胶体 |
| D.向电石中缓慢滴入饱和食盐水,可制取C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
向饱和澄清石灰水中加入少量CaC2,充分反应后恢复到原来的温度,所得溶液中
| A.c(Ca2+)、c(OH-)均增大 | B.c(Ca2+)、c(OH-)均保持不变 |
| C.c(Ca2+)、c(OH-)均减小 | D.c(OH-)增大、c(H+)减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com