
| A£® | Cl2 | B£® | Na2O2 | C£® | Na2O | D£® | NaOH |
·ÖĪö A£®Cl2ŗĶĖ®·“Ӧɜ³ÉHClŗĶHClO£»
B£®¹żŃõ»ÆÄĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆÄĘŗĶŃõĘų£»
C£®Ńõ»ÆÄĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆÄĘ£»
D£®NaOHŗĶĖ®²»·“Ó¦£®
½ā“š ½ā£ŗA£®Cl2ŗĶĖ®·“Ӧɜ³ÉHClŗĶHClO£¬·½³ĢŹ½ĪŖ£ŗCl2+H2O?HCl+HClO£¬¹ŹA²»Ń”£»
B£®¹żŃõ»ÆÄĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆÄĘŗĶŃõĘų£¬·½³ĢŹ½ĪŖ£ŗ2Na2O2+2H2O=4NaOH+O2”ü£¬¹ŹB²»Ń”£»
C£®Ńõ»ÆÄĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆÄĘ£¬·½³ĢŹ½ĪŖ£ŗNa2O+H2O=NaOH£¬¹ŹC²»Ń”£»
D£®NaOHŗĶĖ®²»·“Ó¦£¬¹ŹDŃ”£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖÄĘ¼°Ęä»ÆŗĻĪļµÄŠŌÖŹ£¬Ć÷Č·ĪļÖŹµÄŠŌÖŹŹĒ½ā±¾Ģā¹Ų¼ü£¬ÄŃ¶Č²»“ó£®


 Š”ѧæĪŹ±×÷ŅµČ«ĶØĮ·°øĻµĮŠ“š°ø
Š”ѧæĪŹ±×÷ŅµČ«ĶØĮ·°øĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 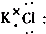 | B£® | 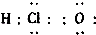 | ||
| C£® | 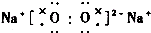 | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬56gÓÉN2ŗĶCO×é³ÉµÄ»ģŗĻĘųĢåŗ¬ÓŠµÄŌ×ÓŹżÄæĪŖ4 NA | |
| B£® | øßĪĀĻĀ£¬0.2 molFeÓė×ćĮæĖ®ÕōĘų·“Ó¦£¬Éś³ÉµÄH2·Ö×ÓŹżĪŖ0.3NA | |
| C£® | 1 L 1.0mol•L-1µÄNaAlO2Ė®ČÜŅŗÖŠŗ¬ÓŠµÄ×ÜŌ×ÓŹżĪŖ2NA | |
| D£® | 1 molōĒ»łÖŠŗ¬ÓŠµÄµē×ÓŹżĪŖ10NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŹµŃé²Ł×÷ | Ō¤²āµÄŹµŃéĻÖĻó | ŹµŃé½įĀŪ»ņ½āŹĶ | |
| A | Ļņ±„ŗĶNa2CO3 ČÜŅŗÖŠµĪ¼ÓÉŁĮæĻ”ŃĪĖį | Į¢¼“ÓŠĘųĢåŅŻ³ö | CO32-+2H+ØTH2O+CO2”ü |
| B | ½«ÅØĮņĖįµĪ¼Óµ½Ź¢ÓŠĶʬµÄŹŌ¹ÜÖŠ£¬²¢½« ÕŗÓŠĘ·ŗģČÜŅŗµÄŹŌÖ½ÖĆÓŚŹŌ¹ÜæŚ | Ę·ŗģŹŌÖ½ĶŹÉ« | SO2¾ßÓŠĘư׊Ō |
| C | ĀĮ²ŌŚ¾Ę¾«µĘ»šŃęÉĻ¼ÓČČ | ĀĮČŪ»Æµ«²»»įµĪĻĀ | A12O3µÄČŪµć±ČĀĮøß |
| D | Ļņµķ·ŪµÄĖįŠŌĖ®½āŅŗÖŠµĪČėÉŁĮæŠĀÖĘ Cu £ØOH£©2Šü×ĒŅŗ²¢¼ÓČČ | ӊשŗģÉ«³ĮµķÉś³É | ĘĻĢŃĢĒ¾ßÓŠ»¹ŌŠŌ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
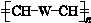 £ØWŹĒĮ“½ŚÖŠµÄ²æ·Ö½į¹¹£©ŹĒŅ»ĄąÖŲŅŖµÄ¹¦ÄÜøß·Ö×Ó²ÄĮĻ£®¾ŪŗĻĪļ XŹĒĘäÖŠµÄŅ»ÖÖ£¬×Ŗ»ÆĀ·ĻßČēĶ¼£ŗ
£ØWŹĒĮ“½ŚÖŠµÄ²æ·Ö½į¹¹£©ŹĒŅ»ĄąÖŲŅŖµÄ¹¦ÄÜøß·Ö×Ó²ÄĮĻ£®¾ŪŗĻĪļ XŹĒĘäÖŠµÄŅ»ÖÖ£¬×Ŗ»ÆĀ·ĻßČēĶ¼£ŗ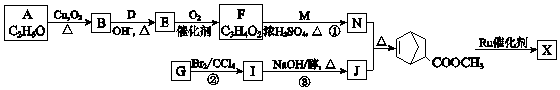
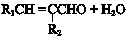
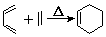
 +2NaOH$”ś_{”÷}^{“¼}$
+2NaOH$”ś_{”÷}^{“¼}$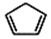 +2 NaBr+2 H2O£®
+2 NaBr+2 H2O£®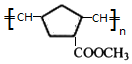 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŠæŹĒøŗ¼«£¬·¢Éś»¹Ō·“Ó¦ | |
| B£® | O2ŌŚÕż¼«·¢ÉśŃõ»Æ·“Ó¦ | |
| C£® | ¹¤×÷Ņ»¶ĪŹ±¼äŗ󣬵ē½āÖŹČÜŅŗµÄ¼īŠŌ»į¼õČõ | |
| D£® | øƵē³ŲÄܽ«»ÆѧÄÜČ«²æ×Ŗ»ÆĪŖµēÄÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ü | B£® | ¢Ś¢Ü | C£® | ¢Ł¢Ü | D£® | ¢Ł¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
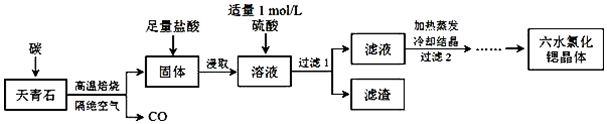
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«10%µÄĘĻĢŃĢĒČÜŅŗ¼ÓČėŠĀÖĘĒāŃõ»ÆĶŠü×ĒŅŗÖŠ£¬¼ÓČČæɵƵ½×©ŗģÉ«³Įµķ | |
| B£® | ±½¼ÓČėµ½äåĖ®ÖŠ£¬±½ŗĶäå·¢ÉśČ”“ś·“Ó¦¶ųŹ¹äåĖ®ĶŹÉ« | |
| C£® | ŌŚ½ą¾»µÄŹŌ¹ÜÖŠ¼ÓČė1”«2 mL AgNO3ČÜŅŗ£¬ŌŁµĪ¼ÓĻ”°±Ė®£¬Ö±µ½AgOHĶźČ«³Įµķ£¬¼“ÖʵĆŅų°±ČÜŅŗ | |
| D£® | ŌŚæÕĘųÖŠ×ĘÉÕĶĖ棬“żĶĖæĄäČ“ŗóÉģČėŅŅ“¼ÖŠ£¬·“ø“¶ą“Ī£¬æÉŅŌÖʵĆŅŅČ© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com