
���� �������ķ���ʽΪCnH2n+2����
CnH2n+2+$\frac{3n+1}{2}$O2$\frac{\underline{\;��ȼ\;}}{\;}$nCO2+��n+1��H2O��g�� ����仯��V
1 $\frac{3n+1}{2}$ n n+1 $\frac{n-1}{2}$
����������仯��ԭ���֮�ȣ�$\frac{��V}{V��������}$=$\frac{n-1}{2}$
��1������V=0����$\frac{n-1}{2}$=0�����n=1��A�ķ���ʽΪCH4��
��2��������B��̼ԭ����ĿΪ��x+1������C��̼ԭ����ĿΪ��2x+1������B�ķ���ʽΪCx+1H2x+4����C�ķ���ʽΪ��C2x+1H4x+4�����������ΪVmL�������������仯��ԭ���֮���з��̼�����
��� �⣺�������ķ���ʽΪCnH2n+2����
CnH2n+2+$\frac{3n+1}{2}$O2$\frac{\underline{\;��ȼ\;}}{\;}$nCO2+��n+1��H2O��g�� ����仯��V
1 $\frac{3n+1}{2}$ n n+1 $\frac{n-1}{2}$
����������仯��ԭ���֮�ȣ�$\frac{��V}{V��������}$=$\frac{n-1}{2}$
��1������V=0����$\frac{n-1}{2}$=0�����n=1��A�ķ���ʽΪCH4����Է�������Ϊ16��
��A�ķ���ʽΪCH4����Է�������Ϊ16��
��2��������B��̼ԭ����ĿΪ��x+1������C��̼ԭ����ĿΪ��2x+1������B�ķ���ʽΪCx+1H2x+4����C�ķ���ʽΪ��C2x+1H4x+4�����������ΪVmL��
����������仯��ԭ���֮�ȣ���ӦB���ʣ�$\frac{4}{V}$=$\frac{x+1-1}{2}$����ӦC���ʣ�$\frac{��V+30����0.25}{V}$=$\frac{2n+1-1}{2}$
������ã�V=2��n=4��
����B�ķ���ʽΪC5H12��C�ķ���ʽΪC9H20��A��B��C�����Ϊ2mL��
�����������Ϊ2mL��B�ķ���ʽΪC5H12��C�ķ���ʽΪC9H20��
���� ���⿼���л������ʽȷ������ȼ���йؼ��㣬�ѶȽϴϺõĿ���ѧ�����������������ҳ���������仯��ԭ���֮��Ĺ�ϵ�ǽ���Ĺؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
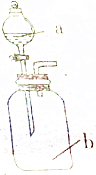 ��ͼ��ʾ���������Լ�a�����Լ�ƿb�У�����ʵ������������ȷ���ǣ�������
��ͼ��ʾ���������Լ�a�����Լ�ƿb�У�����ʵ������������ȷ���ǣ�������| ѡ�� | �Լ�a | �Լ�b | Ԥ��ʵ������ |
| A | Ũ���� | �������� | ������������ɫ���� |
| B | �ռ���Һ | ������Һ | �����ɰ�ɫ���������ܽ� |
| C | Ũ���� | ��Ƭ | ��Ƭ�ܽ⣬������������ɫ���� |
| D | ϡ���� | ��KSCN������������Һ | ��Һ���ɫ����Һ�в������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����� | ʵ��Ŀ�� |
| A | ��ZnS�İ�ɫ��Һ�еμ���CuSO4��Һ | ̽��Ksp��ZnS����Ksp��CuS������Դ�С |
| B | ��pH��ֽ�ֱ�ⶨ��Ũ�ȵ�NaF��NaClO��Һ��pH | ̽��HF��HClO�ĵ��볣�� |
| C | ȡ��������������Һ���μ������KSCN��Һ | ̽�����������Ƿ���� |
| D | ��CH2=CHCH2OH�еμ����Ը��������Һ���� | �����ϩ���Ƿ����̼̼˫�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | S��s��+O2��g���TSO2��g����H=��H2-��H1 | |
| B�� | S��s��+O2��g���TSO2��g����H=��H1-��H2 | |
| C�� | S��s��+O2��g���TSO2��g����H=��H2+��H1 | |
| D�� | 1molS��s��ȼ������1molSO2��g���ų�����������1molS��g��ȼ������1molSO2��g���ų������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �ܢݢ� | C�� | �ڢۢݢ� | D�� | �٢ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
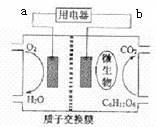
| A�� | ����ٽ��˷�Ӧ�е��ӵ�ת�� | |
| B�� | ����a�ĵ缫Ϊ���� | |
| C�� | �ŵ�����У����ӣ�H+���Ӹ�������������Ǩ�� | |
| D�� | ��صĸ�����ӦΪ��C6H12O6+6H2O-24e-�T6CO2+24H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com