
 现使用酸碱中和滴定法测定市售白醋(CH3COOH)的总酸量(g/100mL).
现使用酸碱中和滴定法测定市售白醋(CH3COOH)的总酸量(g/100mL).| 滴定次数 | 1 | 2 | 3 | 4 |
| V(样品) (mL) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) (mL) | 15.95 | 15.00 | 15.05 | 14.95 |
分析 Ⅰ.(1)溶液的定容在对应体积的容量瓶中进行;
(2)强碱滴定弱酸时应选择碱性变色范围内的指示剂酚酞;
(3)根据滴定管的结构与精确度来分析;
(4)滴定终点的现象是溶液由无色恰好变为浅红色,并在半分钟内不褪色;
Ⅲ.(5)根据数据的合理性来分析;求出平均消耗的NaOH溶液的体积,然后根据白醋与NaOH 溶液反应的关系式来解答.
解答 解:Ⅰ.(1)用滴定管(或10mL移液管)(量取10.00mL食用白醋,在烧杯中用水稀释后转移到100mL 容量瓶中定容,摇匀即得待测白醋溶液,
故答案为:容量瓶;
(2)食醋与NaOH反应生成了强碱弱酸盐,溶液呈碱性,应选择碱性变色范围内的指示剂酚酞,
故答案为:酚酞溶液;
(3)滴定管液面的读数0.70mL,
故答案为:0.70;
(4)滴定终点的现象是溶液由无色恰好变为浅红色,并在半分钟内不褪色,
故答案为:溶液由无色恰好变为浅红色,并在半分钟内不褪色;
Ⅲ.(5)第一组数据与后三组数据相差较大,属于异常值,应舍去;3次消耗的NaOH溶液的体积为:15.00mL;15.05mL;14.95mL;
则NaOH溶液的体积的平均值为15.00mL;
设10mL市售白醋样品含有 CH3COOH Xg,则
CH3COOH~NaOH
60 40
Xg×0.2 0.1000mol/L×0.015L×40g/mol
X=0.4500
样品总酸量为0.450g×$\frac{100mL}{10mL}$=4.500,
故答案为:第一组数据与后三组数据相差较大,属于异常值,应舍去; 4.500.
点评 本题主要考查了中和滴定操作、实验仪器的选择、指示剂的选择等,难度中等,注意把握中和滴定实验的原理.


科目:高中化学 来源: 题型:选择题
| 选项 | X | Y | Z | M |
| A | H2SO4(浓) | Fe2(SO4)3 | FeSO4 | Fe |
| B | O2 | CO2 | CO | C |
| C | Al | Al(OH)3 | NaAlO2 | NaOH |
| D | NaOH | Na2CO3 | NaHCO3 | CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
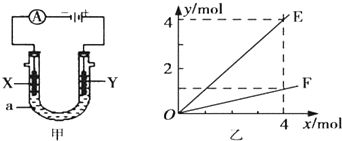
| A. | 若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解的溶液a可以是硫酸铜或氯化铜溶液 | |
| B. | 按图甲装置用惰性电极电解AgNO3溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量 | |
| C. | 按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.5 mol的碳酸铜刚好恢复到通电前的浓度,则电解过程中转移的电子为2.0 mol | |
| D. | 若X、Y为铂电极,a溶液为500 mL KCl和KNO3的混合液,经过一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
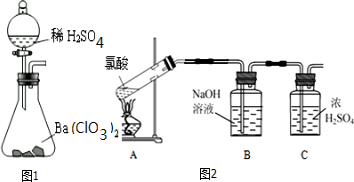
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CCl4、SiCl4、SiH4 | B. | H2S、NF3、CH4 | C. | BCl3、NH3、CO2 | D. | SO3、BF3、H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2═Ba2++2OH- | B. | NaHSO4═Na++HSO4? | ||
| C. | CO32-+2H2O?H2CO3+2OH- | D. | Fe3++3H2O?Fe(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
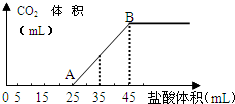 将一定质量的碳酸钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol•L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
将一定质量的碳酸钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol•L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 互为同分异构体且属于芳香烃的有机物的结构简式
互为同分异构体且属于芳香烃的有机物的结构简式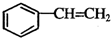 .
. 、
、 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com