
【题目】下列实验操作或对实验事实的叙述正确的是( )
①用稀盐酸洗涤盛放过石灰水的试剂瓶
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;
③有六种分别含Na+、Mg2+、Al3+、Fe2+、Fe3+、NH4+阳离子的溶液,不能用NaOH溶液鉴别;
④用稀硝酸清洗做附着在试管表面的Ag单质;
⑤如果皮肤上不慎沾有浓硫酸,应立即用大量的NaOH稀溶液冲洗;
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物;
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
⑧某溶液加入NaOH并加热能产生使湿润红色石蕊试纸变蓝的气体,则原溶液中含NH4+。
A.①⑤⑦B.③④⑦⑧C.①②④⑧D.②③⑤⑥
【答案】C
【解析】
①石灰水是Ca(OH)2溶液,它与空气中的二氧化碳发生反应生成碳酸钙白色沉淀,碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,所以可以用稀盐酸洗涤盛放过石灰水的试剂瓶,①正确;
②浓硫酸稀释时放热,所以配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌,②正确;
③Na+不与氢氧化钠溶液反应,Mg2+与氢氧化钠溶液反应生成白色沉淀,Al3+与氢氧化钠溶液反应先生成白色沉淀,氢氧化钠过量后沉淀溶解,Fe2+与氢氧化钠溶液反应先生成白色沉淀,白色沉淀逐渐变为灰绿色,最后变为红褐色,Fe3+与氢氧化钠溶液反应生成红褐色沉淀,NH4+与氢氧化钠溶液反应放出具有刺激性气味的气体,混合后现象不同,可用NaOH溶液鉴别,③错误;
④稀硝酸可与银发生反应,所以可用稀硝酸清洗做过银镜反应的试管,④正确;
⑤氢氧化钠具有强腐蚀性,不能用大量的NaOH稀溶液冲洗,如果皮肤上不慎沾有浓硫酸,先用干抹布抹去,再用大量水冲洗,然后用![]() 碳酸氢钠冲洗,⑤错误;
碳酸氢钠冲洗,⑤错误;
⑥瓷坩埚的成分里含有二氧化硅,高温下会与碳酸钠反应:Na2CO3+SiO2=Na2SiO3+ CO2↑,会腐蚀瓷坩埚,所以不能用瓷坩埚,应用铁坩埚,⑥错误;
⑦实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时即可得到氢氧化铁胶体,⑦错误;
⑧氨气溶于水显碱性能使湿润红色石蕊试纸变蓝,所以某溶液中加入NaOH并加热能产生使湿润红色石蕊试纸变蓝的气体,该气体是氨气,原溶液中含NH4+,⑧正确,故答案为:C。


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】室温下,将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)△CuSO4(s)+5H2O(l), 热效应为△H3。则下列判断正确的是
A. △H2>△H3 B. △H1<△H3
C. △H1+△H3=△H2 D. △H1+△H2>△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用滴定管量取一定体积的浓氯水置于锥形瓶中,用NaOH溶液以恒定速度来滴定该浓氯水,根据测定结果绘制出ClO-、ClO3-等离子的物质的量浓度c与时间t的关系曲线如下。下列说法正确的是

A.NaOH溶液和浓氯水可以使用同种滴定管盛装
B.![]() 点溶液中存在如下关系:c(Na+)+ c(H+)=c(ClO-) +c(ClO3-) +c(OH-)
点溶液中存在如下关系:c(Na+)+ c(H+)=c(ClO-) +c(ClO3-) +c(OH-)
C.![]() 点溶液中各离子浓度:c(Na+)> c(Cl-) >c(ClO3-) =c(ClO-)> c(OH-) >c(H+)
点溶液中各离子浓度:c(Na+)> c(Cl-) >c(ClO3-) =c(ClO-)> c(OH-) >c(H+)
D.t2~t4,ClO-的物质的量下降的原因可能是ClO-自身歧化:2 ClO-=Cl-+ClO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某实验小组尝试用燃烧法确定有机物M的分子式,所用装置如下:


①产生的氧气按从左到右方向流动,所选装置各导管的连接顺序是(以上装置不能重复使用):g→fe→hi→ __________ → ___________ →jk。
②F装置作用是________________。
③若准确称取有机物M(只含C、H、O三种元素中的两种或三种)3.24g,经充分燃烧后,A管质量增加9.24g,B管质量增加2.16 g,则该有机物的实验式为________。
④已知在相同条件下该M蒸气相对氢气的密度为54,且能与Na反应但不与NaOH溶液反应,写出该物质在灼热的铜丝条件下与氧气的反应方程式 _________________________________。
(2)在常温下测得的某烃C8H10(不能与溴水反应)的核磁共振谱上,观察到两种类型的H原子给出的信号,其强度之比为2∶3,试确定该烃的结构简式为________;该烃在光照下生成的一氯代物在核磁共振谱中产生的吸收峰强度比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol·L-1FeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压数值):

(1)用KSCN溶液检验出Fe3+的现象是_______________________________________。
(2)Ⅰ中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应: _____________。
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有________性。
(4)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:

①NaCl溶液的浓度是________ mol·L-1。
②Ⅳ中检测Cl2的实验方法:______________________________________________。
③与Ⅱ对比,得出的结论(写出两点):_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)龚老师在大学时候以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:

已知:①Cl2+2OHClO+Cl+H2O是放热反应。
②N2H4·H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
步骤Ⅰ制备NaClO溶液时,若温度超过40℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为_____;实验中控制温度除用冰水浴外,还需采取的措施是_______。
(2)步骤Ⅱ合成N2H4·H2O的装置如图所示。

NaClO碱性溶液与尿素水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。实验中通过滴液漏斗滴加的溶液是_________;使用冷凝管的目的是_____。
(3)紧接着龚老师查阅资料发现AgSCN为白色难溶物,Ag+可以氧化SCNˉ和Fe2+。为探究SCNˉ和Fe2+的还原性强弱,该同学设计了下图实验装置并进行下列实验。

先断开电键K,向溶液X中滴加0.1mol·L-1KSCN溶液,无明显现象,说明___________________;闭合电键K后,若观察到的实验现象有溶液X逐渐变红、右边石墨电极上有固体析出、电流计指针偏转,据此得出的结论是_____,溶液变红的原因是__________________(用离子方程式表示),该实验设计的优点是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2SO2(g)+O2(g) ![]() 2SO3(g) △H <0。请回答下列问题:
2SO3(g) △H <0。请回答下列问题:
(1)某温度下,在一固定体积为2升的密闭容器中,充入2molSO2和lmolO2发生上述反应,当反应进行到2分钟末时达到平衡,平衡混合物中SO3的质量分数为50%,则反应前2分钟内用SO2表示的平均反应速率为_____,SO2的转化率为____,此时反应的平衡常数为_________。
(2)在某恒温、恒压容器中,按体积比2: 1加入SO2和O2进行上述反应,达到平衡后,再向容器中充入适量SO3(g),达到新平衡时,c(O2)将比原平衡_____(填“增大”、“减小”、或“不变”)
(3)若在某恒温、恒容容器中,加入一定量SO3(g)发生上述反应,达到平衡后,再向容器 中充入适量SO3(g),达到新平衡时,c(SO2)/c(SO3)将比原平衡______(填“增大”、“减小”、或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向10 mL 0.1 mol·L-lNaCl溶液和10 mL 0.1 mol·L-lK2CrO4溶液中分别滴加0.1 mol·L-lAgNO3溶液。滴加过程中pM[-lgc(Cl-)或-lgc(CrO42-)]与所加AgNO3溶液体积之间的关系如下图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是
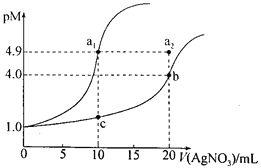
A. 该温度下,Ksp(Ag2CrO4)=4×10-12
B. al、b、c三点所示溶液中c(Ag+):al>b>c
C. 若将上述NaCl溶液浓度改为0.2mol·L-1,则a1点会平移至a2点
D. 用AgNO3标准溶液滴定NaCl溶液时,可用K2CrO4溶液作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,氧化剂与还原剂物质的量之比为1∶2的是 ( )
A. 3S+6NaOH═2Na2S+Na2SO3+3H2O
B. 2CH3COOH+Ca (ClO )2═2HClO+Ca (CH3COO )2
C. I2+2NaClO3═2NaIO3+Cl2
D. 4HCl (浓 )+MnO2![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com