
【题目】化合物E是香料、染料的中间体,一种合成路线如下:
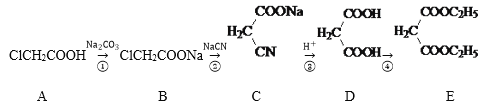
回答下列问题:
(1)A中官能团名称为______________,②的反应类型是___________。1molA与NaOH热溶液充分反应消耗NaOH的物质的量为__________mol。
(2)分别写出反应②和反应④化学方程式。
反应②__________________________________________________
反应④__________________________________________________
(3)写出与D互为同分异构体的含酯基化合物的结构简式____________________。
(4)乙酸甲酯(CH3COOCH3)可用作溶纤剂、喷漆溶剂,以及用于制备人造革。设计由甲醇为起始原料制备乙酸甲酯(CH3COOCH3)的合成路线(无机试剂任选)。合成路线常用的表示方式为:A![]() B
B![]()
![]() 目标产物 ___________________________。
目标产物 ___________________________。
【答案】氯原子、羧基 取代反应 2 ClCH2COONa+NaCN→![]() +NaCl
+NaCl ![]()
![]() CH3OH
CH3OH![]() CH3Cl
CH3Cl![]() CH3CN
CH3CN![]() CH3COOH
CH3COOH![]() CH3COOCH3
CH3COOCH3
【解析】
(1)根据官能团是对化合物的性质起决定作用的原子或原子团,结合ClCH2COOH的结构判断其官能团;根据化合物B、C的结构的区别判断反应类型;利用卤素原子和羧基均可以与NaOH发生反应判断;
(2)反应②是ClCH2COONa与NaCN反应产生NC-CH2-COONa和NaCl;
反应④是丙二酸与乙醇发生酯化反应产生产生酯和水;
(3)根据碳原子数相同的羧酸与酯互为同分异构体书写;
(4)使甲醇先与HCl发生取代反应产生CH3Cl,CH3Cl与NaCN发生取代反应产生CH3CN,然后酸化得到CH3COOH,然后使乙酸与甲醇发生酯化反应产生乙酸甲酯。
(1)ClCH2COOH是氯代乙酸,官能团是氯原子、羧基;B是ClCH2COON,该物质与NaCN发生取代反应,-CN取代-Cl原子得到C:NC-CH2-COONa,ClCH2COOH与NaOH在一定条件下发生反应,产生NaCl、HO-CH2-COONa和水,反应方程式为ClCH2COOH+2NaOH![]() NaCl+HO-CH2-COONa+H2O,所以1molClCH2COOH反应消耗2molNaOH;
NaCl+HO-CH2-COONa+H2O,所以1molClCH2COOH反应消耗2molNaOH;
(2)反应②ClCH2COONa与NaCN反应产生NC-CH2-COONa和NaCl,反应方程式为ClCH2COONa+NaCN![]() NC-CH2-COONa+NaCl;
NC-CH2-COONa+NaCl;
反应④是丙二酸与乙醇发生酯化反应产生产生酯和水,反应的方程式为HOOC-CH2-COOH+2C2H5OH![]()
![]() +2H2O;
+2H2O;
(3)D是HOOC-CH2-COOH,结合碳原子数相同的羧酸与酯互为同分异构体,可知D的含酯基的同分异构体结构简式为HCOOCH2-OOCH;
(4)甲醇与HCl在一定条件下发生取代反应产生CH3Cl,产生的CH3Cl与NaCN发生取代反应产生CH3CN,然后酸化可得乙酸CH3COOH,乙酸与甲醇在浓硫酸存在时,在加热条件下发生酯化反应产生乙酸甲酯和水,因此合成路线为:CH3OH![]() CH3Cl
CH3Cl![]() CH3CN
CH3CN![]() CH3COOH
CH3COOH![]() CH3COOCH3。
CH3COOCH3。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
【题目】根据组成原电池的条件,试以反应:Fe+Cu2+=Fe2++Cu设计一个原电池,画出示意图并标出原电池的正、负极和电子的流向(画在方框中)。_________________
供选用的电解质溶液有:稀硫酸、硫酸铜溶液
供选用的电极材料有:锌片、铜片、铁片
电极材料及电极反应式:
负极材料:______________,电极反应式:___________________,
正极材料:______________,电极反应式:___________________,
电解质溶液:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对伞花烃(图I)常用作染料、医药、香料的中间体。下列说法错误的是
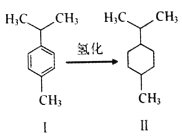
A. 常温对伞花烃呈液态且难溶于水
B. 图Ⅱ物质的一氯代物有5种结构
C. 对伞花烃最多有9个碳原子共平面
D. 图中氢化反应既是加成反应又是还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将同温同压下的H2、O2、Cl2按13:6:1的体积比混合,在密闭容器中用电火花引燃,充分反应后使产物冷却液化,所得溶液的质量分数是( )
A.33.6%B.25.3%C.16.8%D.14.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2、Na2S2O3、Na2S、Na2SO3、Na2SO4等含硫化合物在工业上有广泛的用途。完成下列填空:
(1)硫原子最外层电子排布式_______________,钠原子的核外有______种能量不同的电子。Na2S的电子式____________。
(2)涉及元素形成简单离子半径大小顺序:__________________;请用原子结构知识说明氧与硫的非金属性强弱________________________________________________________。
(3)棉织物用氯气漂白后,加入Na2S2O3除去余氯时,发生如下反应:
____S2O32-+____Cl2+____H2O→____SO42-+____Cl-+____H+,配平该反应方程式:若反应中生成2molSO42-,则转移电子_____mol。
(4)Na2S又称臭碱,用离子方程式说明Na2S溶液呈碱性的原因________。 SO2分子构型“V”形,则SO2是_____(选填“极性”、“非极性”)分子。列举一个实验事实说明SO2具有还原性_________。
(5)图是Na2SO3溶液中各离子浓度的相对大小关系示意图。其中,②是____________(填微粒符号)。上述5种物质中,不能促进也不能抑制水电离的化合物____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是
A. PM2.5和PM10都是空气质量指数(AQI)的重要指标
B. 汽车尾气中的NO2和CO2都是大气污染
C. 聚乙烯和聚氯乙烯随意乱扔都能产生白色污染
D. 含N和P的大量污水任意排放都能导致水体富营养化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室验证钠能与二氧化碳发生反应,并确定其产物的装置如图所示(已知:PdC12溶液遇CO能产生黑色的Pd),下列说法错误的是

A. 装置①的仪器还可以制取H2、NH3等气体
B. 装置⑤中石灰水变浑浊后,再点燃酒精灯
C. 装置②③中分别盛装饱和Na2CO3溶液、浓H2SO4
D. 装置⑥中有黑色沉淀,发生的反应是PdC12+CO+H2O=Pd↓+CO2+2HC1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积一定的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g) + bB(g)![]() xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指( )
xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指( )

A.反应物A的百分含量
B.平衡混合气中物质B的百分含量
C.平衡混合气的密度
D.平衡混合气的平均摩尔质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】12.4gNa2X中含有0.4molNa+,则Na2X的摩尔质量是___________,它的相对分子质量是___________,X的相对原子质量是__________,该物质的化学式__________。有一种气体的质量为14.2 g,体积是4.48 L(标准状况),该气体的摩尔质量是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com