
【题目】2005年诺贝尔化学奖授予了研究烯烃复分解反应的科学家,以表彰他们作出的卓越贡献。烯烃复分解反应原理如下:C2H5CH=CHCH3+CH2=CH2![]() C2H5CH=CH2+CH2=CHCH3
C2H5CH=CH2+CH2=CHCH3
现以烯烃C5H10为原料,合成有机物M和N,合成路线如下:

(1)按系统命名法,有机物A的名称是_______。
(2)B的结构简式是__________。
(3)C![]() D的反应类型是___________。
D的反应类型是___________。
(4)写出D![]() M的化学方程式________。
M的化学方程式________。
(5)已知X的苯环上只有一个取代基,且取代基无甲基,则N的结构简式为_______。
(6)满足下列条件的X的同分异构体共有_______种,写出任意一种的结构简式_________。
①遇FeCl3溶液显紫色 ②苯环上的一氯取代物只有两种
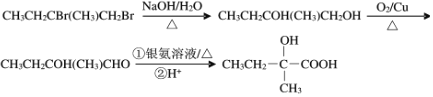
(7)写出E![]() F合成路线(用结构简式表示有机物,箭头上注明试剂和反应条件)。______
F合成路线(用结构简式表示有机物,箭头上注明试剂和反应条件)。______
![]()
【答案】2-甲基-1-丁烯 CH3CH2C(CH3)=C(CH3)CH2CH3 取代反应 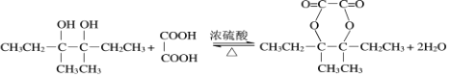
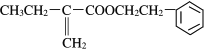 3
3 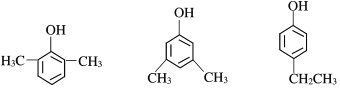
【解析】
由F的结构简式可知A应为CH2=C(CH3)CH2CH3,生成E为CH2BrCBr(CH3)CH2CH3,F发生消去反应生成G,G为![]() ,X的苯环上只有一个取代基,且取代基无甲基,结合N的分子式可知N的结构简式为
,X的苯环上只有一个取代基,且取代基无甲基,结合N的分子式可知N的结构简式为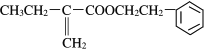 ,可知X为苯乙醇,由M的分子式可知D含有8个C,结合信息可知B为CH3CH2C(CH3)=C(CH3)CH2CH3,则C为CH3CH2CBr(CH3)CBr(CH3)CH2CH3,D为CH3CH2COH(CH3)COH(CH3)CH2CH3,M为
,可知X为苯乙醇,由M的分子式可知D含有8个C,结合信息可知B为CH3CH2C(CH3)=C(CH3)CH2CH3,则C为CH3CH2CBr(CH3)CBr(CH3)CH2CH3,D为CH3CH2COH(CH3)COH(CH3)CH2CH3,M为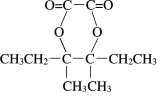 ,以此解答该题。
,以此解答该题。
(1)A为CH2=C(CH3)CH2CH3,名称为2-甲基-1-丁烯;
(2)由以上分析可知B为CH3CH2C(CH3)=C(CH3)CH2CH3;
(3)C为CH3CH2CBr(CH3)CBr(CH3)CH2CH3,在氢氧化钠溶液中发生取代反应生成CH3CH2COH(CH3)COH(CH3)CH2CH3,故反应类型为取代反应;
(4)D为CH3CH2COH(CH3)COH(CH3)CH2CH3,M为 ,反应的方程式为
,反应的方程式为 ;
;
(5)由以上分析可知N为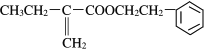 ;
;
(6)X为苯乙醇,对应的同分异构体①遇FeCl3溶液显紫色,则羟基连接在苯环,②苯环上的一氯取代物只有两种,另一取代基为2个甲基或1个乙基,共3种,即 等;
等;
(7)E为CH2BrCBr(CH3)CH2CH3,可先水解生成CH2OHCOH(CH3)CH2CH3,在铜催化条件下被氧化生成醛,然后与弱氧化剂反应生成酸,反应的流程为 。
。


科目:高中化学 来源: 题型:
【题目】NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
(1)实验室用金属铜和稀硝酸制取NO的离子方程式为_________________________________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填选项编号)。
A 铁 B 铝 C 铂 D 玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是____________________(填化学方程式)。
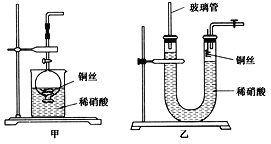
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是_____________________________________________________。
②让反应停止的操作方法及原因是________________________________________。
(4)以下收集NO气体的装置,
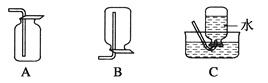
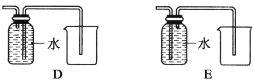
合理的是________(填选项代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学向一定体积的Ba(OH)2溶液中逐渐加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。该小组的同学关于如图的下列说法中,不正确的是( )
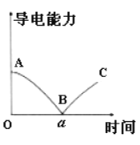
A.AB段溶液的导电能力不断减弱,说明生成的BaSO4不是电解质
B.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
C.BC段溶液的导电能力不断增大,主要是由于过量的H2SO4电离出的离子导电
D.a时刻Ba(OH)2溶液与稀硫酸恰好完全中和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,电解质溶液的性质与变化是多样的,下列说法正确的是( )
A. pH相同的①CH3COONa ②NaClO ③NaOH三种溶液c(Na+)大小:①>②>③
B. 往稀氨水中加水,![]() 的值变小
的值变小
C. pH=4的H2S溶液与pH=10的NaOH溶液等体积混合,存在下列等式:c(Na+)+c(H+)c=(OH—)+2c(S2—)
D. Ca(ClO)2溶液中通入少量CO2,ClO—水解程度增大,溶液碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 1mol任何气体的体积都是22.4L
B. 同温同压下两种气体,只要它们的分子数相同,所占体积也一定相同
C. 在标准状况下,体积为22.4L的物质都是1mol
D. 在非标准状况下,1mol任何气体的体积不可能是22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 64 g SO2含有氧原子数为1NA
B. 物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为1 NA
C. 标准状况下,22.4 L H2O的分子数为1NA
D. 常温常压下,14 g N2含有分子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.23 g钠的原子最外层电子数为2NAB.1 L 0.1 mol·L-1乙酸溶液中H+数为0.1NA
C.标准状况下,22.4 L乙烷的分子数为NAD.1 mol羟基所含电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2,则关于该反应体系说法错误的是
A.该反应的化学方程式为2H2CrO4+3H2O2=2Cr(OH)3+3O2↑+2H2O
B.该反应中的氧化剂是H2O2,还原产物是O2
C.氧化性:H2CrO4>O2
D.如反应转移了0.3 rnol电子,则产生的气体在标准状况下体积为3.36 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl2溶液有时呈黄色,有时呈绿色或蓝色,这是因为在CuCl2的水溶液中存在如下平衡:
[Cu(H2O)4]2++4Cl-![]() [CuCl4]2-+4H2O
[CuCl4]2-+4H2O
蓝色 绿色
欲使溶液由绿色变为蓝色,可采用的方法是( )
A. 加NaCl溶液B. 加水C. 加AgNO3溶液D. 加NaOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com