
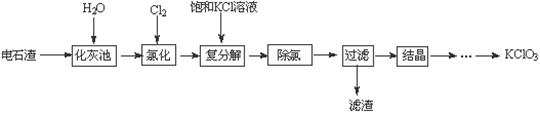
实验室利用电石渣(主要含CaO、CaC2及少量C、SiO2)为原料制备氯酸钾的实验流程及相关物质的溶解度如下:
| 几种物质溶解度与温度的关系 | |||||
| 温度 | 0 | 10 | 20 | 30 | 40 |
| S(CaCl2)/g | 59.5 | 64.7 | 74.5 | 100 | 128 |
| S[Ca(ClO3)2]/g | 209 | ||||
| S(KClO3)/g | 3.3 | 5.2 | 7.3 | 10.2 | 13.9 |
(1) 化灰池中CaC2与水反应的化学方程式为 。
(2)在80℃氯化时产生氯酸钙及氯化钙的化学方程式为 ;除去溶液中多余的氯气的简单方法是 。
(3)饱和KCl溶液能与氯酸钙反应的原因是 。
(4)滤渣中的成分主要是 (写化学式);从过滤后的溶液中获得KClO3晶体的方法是 、 、洗涤、烘干。
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
糖尿病是由于人体内胰岛素紊乱导致的代谢紊乱综合症,以高血糖为主要标志。长期摄入高热量食品和缺少运动都易导致患糖尿病。
(1)血糖是指血液中的葡萄糖,下列说法正确的是________(填序号)。
A.葡萄糖属于碳水化合物,分子式可表示为C6(H2O)6,则每个葡萄糖分子中含6个H2O分子
B.可用新制的氢氧化铜悬浊液来检测糖尿病病人尿液中的葡萄糖含量
C.葡萄糖可用于制镜工业
D.淀粉、纤维素水解的最终产物都是葡萄糖
(2)木糖醇是一种甜味剂,糖尿病病人食用后不会使血糖升高。木糖醇与葡萄糖________(填“互为”或“不互为”)同分异构体。请预测木糖醇的一种化学性质:________。
(3)糖尿病病人不可饮酒,酒精在肝脏内可被转化成有机物A。已知A的相对分子质量为60;将A溶于水,滴入石蕊试液,发现溶液变红。则A的结构简式为_____________________________________________ ___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是 ( )
A.浓硝酸中加入过量铁粉并加热:Fe+3NO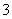 +6H+=Fe3++3NO2↑+3H2O
+6H+=Fe3++3NO2↑+3H2O
B.Ca(HCO3)2溶液与过量NaOH溶液反应 HCO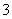 +OH-+Ca2+===CaCO3↓+H2O
+OH-+Ca2+===CaCO3↓+H2O
C.氢氧化铁溶于氢碘酸溶液:Fe(OH)3+3H+===Fe3++3H2O
D.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:
Ba2++2OH-+NH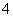 +HCO
+HCO ===BaCO3↓+NH3·H2O+H2O
===BaCO3↓+NH3·H2O+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质性质与应用对应关系正确的是
A.氨气具有碱性,可用作制冷剂
B.二氧化硅能与氢氟酸反应,可用于生产光导纤维
C.铝具有良好导电性和耐腐蚀性,可用于制作高压输电线
D.二氧化铅具有强氧化性,可用于铅蓄电池的负极材料
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.镀层破损后白铁(镀锌铁)比马口铁(镀锡铁)中的铁更易腐蚀
B.SO2(g) + 2H2S(g) = 3S(s)+2H2O(l) 在常温下能自发进行,则该反应的△H>0
C.0.1 mol·L-1CH3COOH溶液中加入少量水,CH3COOH电离程度和溶液pH均增大
D.在N2+3H2 2NH3平衡体系中加入少量催化剂,反应速率和平衡常数均增大
2NH3平衡体系中加入少量催化剂,反应速率和平衡常数均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
自从1985年发现了富勒烯以来,由于其具有独特的物理和化学性质,越来越受到人
们的关注。
(1)富勒烯(C60)在液相中用FeCl3催化可生成二聚体,过程见图21A—1。
 |
①Fe3+基态时核外电子排布式为 ;
②1molC60分子中含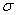 键数目为 ;
键数目为 ;
③富勒烯二聚体中碳原子杂化轨道类型有 。
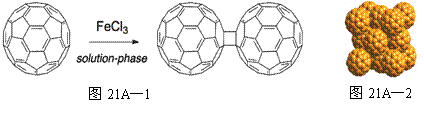
(2)C60的晶胞结构如图21A—2,则与每个C60分子紧邻的C60分子有 个。
(3)我国科学家发现杯[8]芳烃(如图21A—3所示)能与C60形成包合物(如图21A—4),
①杯[8]芳烃底部8个羟基间的作用为 ;
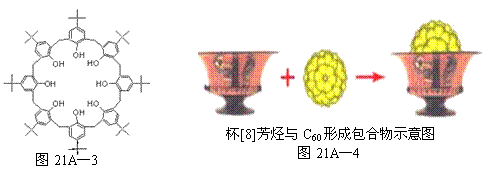 ②杯[8]芳烃包合物中C60与杯芳烃间的作用力为 。
②杯[8]芳烃包合物中C60与杯芳烃间的作用力为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
运用化学反应原理研究元素及其化合物的反应有重要意义。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+ O2(g) 2SO3(g),混合体系中SO3的百分含量和温度的关系如右图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如右图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:

①2SO2(g) + O2(g) 2SO3(g)的△H____0(填“>”、“<”)。若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡 移动(填“向左”“向右”或“不移动”) 。
2SO3(g)的△H____0(填“>”、“<”)。若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡 移动(填“向左”“向右”或“不移动”) 。
②若温度为T1时,反应进行到状态D时,V正_______V逆(填“>”“<”或“=”)
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产中有重要作用。
① 右图是一定的温度和压强下N2和H2反应生成lmolNH3过程中能量变化示意图,请写出工业合成氨的热化学方程式:(△H用含字母Q1、Q2的代数式表示) 。

②在AlCl3溶液中滴加氨水,反应的离子方程式为: 。
(3)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合态存在。在25℃下,向0.1mol•L-1的NaCl溶液中逐滴加入适量的0.1mol•L-1硝酸银溶液,有白色沉淀生成,向反应后的浊液中,继续加入0.1mol•L-1的NaI溶液,看到的现象是 全品教学网, 用后离不了!,产生该现象的原因是(用离子方程式表示): 。
全品教学网, 用后离不了!(已知25℃时Ksp[AgCl] =1.0×10-10 mol2•L-2,Ksp[AgI] =1.5×10-16mol2•L-2 )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验中能证明某气体为SO2的是( )
①使澄清石灰水变浑浊 ②使湿润的蓝色石蕊试纸变红 ③使品红溶液褪色 ④通入足量NaOH溶液中,再滴加BaCl2溶液,有白色沉淀生成,该沉淀溶于稀盐酸 ⑤通入溴水中,能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生
A.都能证明 B.都不能证明
C.③④⑤均能证明 D.只有⑤能证明
查看答案和解析>>
科目:高中化学 来源: 题型:
物质间纷繁复杂的转化关系是化学的魅力所在,下列选项中物质的转化在一定条件下不能实现的是( )。
| 选项 | 转化关系 |
| A | Si |
| B | NO2 |
| C | Fe |
| D | S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com