
ΓΨΧβΡΩΓΩ![]() «ΙΛ“Β…œ≥Θ”ΟΒΡΝρΜ·ΦΝΘ§“―÷Σ
«ΙΛ“Β…œ≥Θ”ΟΒΡΝρΜ·ΦΝΘ§“―÷Σ![]() ÷–Νρ‘ΣΥΊœ‘
÷–Νρ‘ΣΥΊœ‘![]() ΦέΘ§Υϋ≤ΜΈ»Ε®Θ§‘ΎΥ°÷–“ΉΖΔ…ζαΣΜ·Ζ¥”ΠΘ§“Ή»ή”Ύ”–Μζ»ήΦΝΓΘ Β―ι “≥Θ”Ο
ΦέΘ§Υϋ≤ΜΈ»Ε®Θ§‘ΎΥ°÷–“ΉΖΔ…ζαΣΜ·Ζ¥”ΠΘ§“Ή»ή”Ύ”–Μζ»ήΦΝΓΘ Β―ι “≥Θ”Ο![]() ”κ¥ΩΨΜΒΡ¬»Τχ÷Τ±Η
”κ¥ΩΨΜΒΡ¬»Τχ÷Τ±Η![]() ΓΘΖ¥”Π…φΦΑΒΫΒΡΦΗ÷÷Έο÷ ΒΡ»έΖ–Βψ»γœ¬ΘΚ
ΓΘΖ¥”Π…φΦΑΒΫΒΡΦΗ÷÷Έο÷ ΒΡ»έΖ–Βψ»γœ¬ΘΚ
Έο÷ |
|
|
|
|
Ζ–Βψ | 47 |
| 77 | 137 |
»έΒψ |
|
|
|
|
Β―ι “άϊ”Οœ¬Ν–ΉΑ÷Ο÷Τ±Η![]() (≤ΩΖ÷Φ–≥÷“«ΤςΦΚ¬‘»Ξ)ΘΚ
(≤ΩΖ÷Φ–≥÷“«ΤςΦΚ¬‘»Ξ)ΘΚ
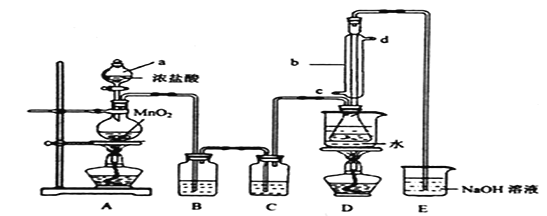
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)ΉΑ÷Ο÷–b≤ΘΝß“«ΤςΒΡΟϊ≥ΤΈΣ_________ΘΜ–¥≥ω÷Τ±Η![]() ΒΡΜ·―ßΖΫ≥Χ Ϋ_________ΓΘ
ΒΡΜ·―ßΖΫ≥Χ Ϋ_________ΓΘ
(2)D÷–≤…”Ο»»Υ°‘ΓΦ”»»ΒΡ‘≠“ρ « _________Θ§Ζ¥”ΠΫα χΚσ¥”ΉΕ–ΈΤΩΡΎΜλΚœΈο÷–Ζ÷άκ≥ω≤ζΤΖΒΡΖΫΖ® «______ΓΘ
(3) Β―ιΙΐ≥Χ÷–Θ§»τ»±…ΌCΉΑ÷ΟΘ§‘ρΖΔœ÷≤ζΤΖΜκΉ«≤Μ«εΘ§≥ωœ÷ΗΟœ÷œσΒΡ‘≠“ρΜ·―ßΖΫ≥Χ Ϋ±μ ΨΈΣ______________ΓΘ
(4)ΗΟ Β ΦΉΑ÷Ο…ηΦΤ¥φ‘Ύ»±œίΘ§ΡψΒΡΗΡΫχΫ®“ι « _________________________________ΓΘ
ΓΨ¥πΑΗΓΩ÷±–ΈάδΡΐΙή ![]() ±ήΟβ≤ζΈο
±ήΟβ≤ζΈο![]() ΤϊΜ· ’τΝσ
ΤϊΜ· ’τΝσ ![]() ‘ΎDΚΆE÷°Φδ‘ωΦ”Η…‘οΉΑ÷Ο
‘ΎDΚΆE÷°Φδ‘ωΦ”Η…‘οΉΑ÷Ο
ΓΨΫβΈωΓΩ
(1)ΗυΨί“«ΤςΒΡΙΙ‘λΖ÷ΈωΘ§”Ο![]() ”κ¥ΩΨΜΒΡ¬»ΤχΖ¥”Π…ζ≥…
”κ¥ΩΨΜΒΡ¬»ΤχΖ¥”Π…ζ≥…![]() ΚΆ
ΚΆ![]() ΘΜ
ΘΜ
(2)ΗυΨί±μ÷– ΐΨίΫαΚœΖ–Βψ≈–ΕœΘΜ
(3)“άΨί‘≠Ή” ΊΚψΓΔΒγΉ” ΊΚψ–¥≥ωΜ·―ßΖΫ≥Χ ΫΘΜ
(4)ΗυΨί![]() ”κΥ°Ζ¥”ΠΒΡ‘≠άμ…ηΦΤΓΘ
”κΥ°Ζ¥”ΠΒΡ‘≠άμ…ηΦΤΓΘ
(1)ΉΑ÷ΟbΈΣάδΡΐΙήΘ§”Ο![]() ”κ¥ΩΨΜΒΡ¬»Τχ÷Τ±Η
”κ¥ΩΨΜΒΡ¬»Τχ÷Τ±Η![]() ΒΡΜ·―ßΖΫ≥Χ ΫΈΣ
ΒΡΜ·―ßΖΫ≥Χ ΫΈΣ![]() Θ§Ι ¥πΑΗΈΣΘΚάδΡΐΙήΘΜ
Θ§Ι ¥πΑΗΈΣΘΚάδΡΐΙήΘΜ![]() ΘΜ
ΘΜ
(2)ΗυΨί±μ÷–Έο÷ ΒΡΖ–ΒψΗΏΒΆΘ§ΈΣΝΥ Ι![]() ΤΫΈ»ΤϊΜ·Θ§±ήΟβ≤ζΈο
ΤΫΈ»ΤϊΜ·Θ§±ήΟβ≤ζΈο![]() ΤϊΜ·Θ§Ω…“‘≤…”ΟΥ°‘ΓΦ”»»ΒΡΖΫΖ®ΘΜΗυΨίΈο÷ ΒΡ»έΖ–ΒψΘ§¥”ΉΕ–ΈΤΩΡΎΜλΚœΈο÷–Ζ÷άκ≥ω
ΤϊΜ·Θ§Ω…“‘≤…”ΟΥ°‘ΓΦ”»»ΒΡΖΫΖ®ΘΜΗυΨίΈο÷ ΒΡ»έΖ–ΒψΘ§¥”ΉΕ–ΈΤΩΡΎΜλΚœΈο÷–Ζ÷άκ≥ω![]() ΒΡΖΫΖ® «’τΝσΘ§ΩΊ÷ΤΈ¬Ε»‘Ύ
ΒΡΖΫΖ® «’τΝσΘ§ΩΊ÷ΤΈ¬Ε»‘Ύ![]() Θ§
Θ§
Ι ¥πΑΗΈΣΘΚ±ήΟβ≤ζΈο![]() ΤϊΜ·ΘΜ’τΝσΘΜ
ΤϊΜ·ΘΜ’τΝσΘΜ
(3)»τ»±…ΌCΉΑ÷ΟΘ§‘ρ¬»Τχ÷–Μλ”–Υ°’τΤχΘ§![]() ‘ΎΥ°÷–ΖΔ…ζαΣΜ·Ζ¥”ΠΘ§”–Έό…Ϊ¥ΧΦΛ–‘ΤχΈΕΤχΧε≤ζ…ζΘ§≤Δ”–ΜΤ…Ϊ≥ΝΒμ…ζ≥…Θ§Έό…Ϊ¥ΧΦΛ–‘ΤχΈΕΤχΧε≥ΐ¬»Μ·«βΆβΘ§“άΨί―θΜ·ΜΙ‘≠Ζ¥”ΠΒΡ‘ΣΥΊΜ·ΚœΦέ±δΜ· ΊΚψΆΤΕœΘ§Μ·ΚœΦέΫΒΒΆΒΡ…ζ≥…ΜΤ…Ϊ≥ΝΒμΈΣΒΞ÷ ΝρΘ§Μ·ΚœΦέ…ΐΗΏΒΡ…ζ≥…Εΰ―θΜ·ΝρΤχΧεΘ§“άΨί‘≠Ή” ΊΚψΓΔΒγΉ” ΊΚψ–¥≥ωΜ·―ßΖΫ≥Χ ΫΈΣΘΚ
‘ΎΥ°÷–ΖΔ…ζαΣΜ·Ζ¥”ΠΘ§”–Έό…Ϊ¥ΧΦΛ–‘ΤχΈΕΤχΧε≤ζ…ζΘ§≤Δ”–ΜΤ…Ϊ≥ΝΒμ…ζ≥…Θ§Έό…Ϊ¥ΧΦΛ–‘ΤχΈΕΤχΧε≥ΐ¬»Μ·«βΆβΘ§“άΨί―θΜ·ΜΙ‘≠Ζ¥”ΠΒΡ‘ΣΥΊΜ·ΚœΦέ±δΜ· ΊΚψΆΤΕœΘ§Μ·ΚœΦέΫΒΒΆΒΡ…ζ≥…ΜΤ…Ϊ≥ΝΒμΈΣΒΞ÷ ΝρΘ§Μ·ΚœΦέ…ΐΗΏΒΡ…ζ≥…Εΰ―θΜ·ΝρΤχΧεΘ§“άΨί‘≠Ή” ΊΚψΓΔΒγΉ” ΊΚψ–¥≥ωΜ·―ßΖΫ≥Χ ΫΈΣΘΚ![]() Θ§
Θ§
Ι ¥πΑΗΈΣΘΚ![]() ΘΜ
ΘΜ
(4)ΈΣΝΥΖά÷ΙΉΑ÷ΟE÷–ΒΡΥ°’τΤχ―ΊΒΦΙήΫχ»κΉΕ–ΈΤΩΘ§![]() ”κΥ°Ζ¥”ΠΘ§≤ζ¬ ΫΒΒΆΘ§”Π‘ΎDΚΆE÷°Φδ‘ωΦ”Η…‘οΉΑ÷ΟΘ§
”κΥ°Ζ¥”ΠΘ§≤ζ¬ ΫΒΒΆΘ§”Π‘ΎDΚΆE÷°Φδ‘ωΦ”Η…‘οΉΑ÷ΟΘ§
Ι ¥πΑΗΈΣΘΚ‘ΎDΚΆE÷°Φδ‘ωΦ”Η…‘οΉΑ÷ΟΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≥τ―θΚήΕύ Β”ΟΧΊ–‘Θ§Τδ«Ω―θΜ·–‘≥Θ”Ο”ΎœϊΕΨ…±ΨζΚΆΖάΗ·±Θœ ΓΘΡΩ«Α÷Τ»Γ≥τ―θΒΡΖΫΖ®ΚήΕύΘ§Τδ÷–ΗΏ―ΙΖ≈ΒγΖ®(DBD)ΚΆΒγΫβ¥ΩΥ°Ζ®‘≠άμ»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®÷–¥μΈσΒΡ «

A.ΝΫ÷÷ΖΫΖ®ΕΦ «ΫΪΒγΡήΉΣΜ·ΈΣΜ·―ßΡή
B.ΗΏ―ΙΖ≈ΒγΖ®ΚΆΒγΫβ¥ΩΥ°Ζ®œύ±»Θ§Μα≤ζ…ζΈέ»Ψ–‘ΒΡNOxΤχΧε
C.ΒγΫβ¥ΩΥ° ±Θ§―τΦΪΖΔ…ζΒΡΒγΦΪΖ¥”Π”–3H2OΘ≠6eΘ≠ΘΫO3ΓϋΘΪ6HΘΪ
D.ΒγΫβ¥ΩΥ° ±Θ§HΘΪ”…ΒγΦΪbΝςœρΒγΦΪa
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΦΉ¥ΦΩ…ΉςΈΣ»ΦΝœΒγ≥ΊΒΡ‘≠ΝœΓΘCO2ΚΆCOΩ…ΉςΈΣΙΛ“ΒΚœ≥…ΦΉ¥ΦΘ®CH3OHΘ©ΒΡ÷±Ϋ”ΧΦ‘¥Θ§
Θ®1Θ©“―÷Σ‘Ύ≥ΘΈ¬≥Θ―Ιœ¬ΘΚ
ΔΌCH3OHΘ®lΘ©+ O2Θ®gΘ©=COΘ®gΘ© + 2H2OΘ®gΘ©ΘΜ ΠΛHΘΫ©¹355.0 kJ®Mmol
ΔΎ2COΘ®gΘ©+ O2Θ®gΘ©= 2CO2Θ®gΘ© ΠΛHΘΫΘ≠566.0 kJ/mol
ΔέH2OΘ®lΘ©=H2OΘ®gΘ© ΠΛHΘΫ+44.0 kJ/mol
–¥≥ω±μ ΨΦΉ¥Φ»Φ…’»»ΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΚ___________________________
Θ®2Θ©άϊ”ΟCOΚΆH2‘Ύ“ΜΕ®ΧθΦΰœ¬Ω…Κœ≥…ΦΉ¥ΦΘ§ΖΔ…ζ»γœ¬Ζ¥”ΠΘΚCOΘ®gΘ©ΘΪ2H2Θ®gΘ©=CH3OHΘ®gΘ©Θ§ΤδΝΫ÷÷Ζ¥”ΠΙΐ≥Χ÷–ΡήΝΩΒΡ±δΜ·«ζœΏ»γœ¬ΆΦaΓΔbΥυ ΨΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «__________
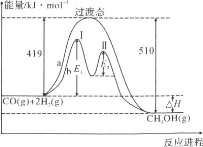
AΘ°…œ ωΖ¥”ΠΒΡΠΛHΘΫΘ≠91kJΓΛmolΘ≠1
BΘ°aΖ¥”Π’ΐΖ¥”ΠΒΡΜνΜ·ΡήΈΣ510kJΓΛmolΘ≠1
CΘ°bΙΐ≥Χ÷–ΒΎΔώΫΉΕΈΈΣΈϋ»»Ζ¥”ΠΘ§ΒΎΔρΫΉΕΈΈΣΖ≈»»Ζ¥”Π
DΘ°bΙΐ≥Χ Ι”Ο¥ΏΜ·ΦΝΚσΫΒΒΆΝΥΖ¥”ΠΒΡΜνΜ·ΡήΚΆΠΛH
EΘ°bΙΐ≥ΧΒΡΖ¥”ΠΥΌ¬ ΘΚΒΎΔρΫΉΕΈΘΨΒΎΔώΫΉΕΈ
Θ®3Θ©œ¬Ν– «ΩΤ―––ΓΉι…ηΦΤΒΡ“ΜΗωΦΉ¥Φ»ΦΝœΒγ≥ΊΘ§ΝΫ±ΏΒΡ“θ”Α≤ΩΖ÷ΈΣaΘ§bΕη–‘ΒγΦΪΘ§Ζ÷±π”ΟΒΦœΏ”κ…’±≠ΒΡmΘ§nœύΝ§Ϋ”Θ§ΙΛΉς‘≠άμ Ψ“βΆΦ»γΆΦΘΚ
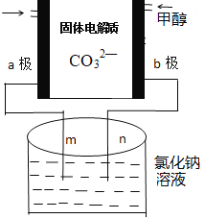
ΔΌbΦΪΒγΦΪΖ¥”Π ΫΈΣ____________ΓΘ
ΔΎ‘Ύ±ξΉΦΉ¥Ωωœ¬Θ§»τΆ®»κ112mLΒΡO2Θ§Θ®ΦΌ…η…’±≠÷–ΒΡ»ή“ΚΒΡΧεΜΐΈΣ200mLΘ§ΧεΜΐ≤Μ±δΘ©ΉνΚσΖ¥”Π÷’÷Ι ±…’±≠÷–»ή“ΚΒΡpHΈΣ______ΓΘ
Θ®4Θ©Ω…άϊ”ΟCO2ΗυΨίΒγΜ·―ß‘≠άμ÷Τ±ΗΥήΝœΘ§Φ»Φθ…ΌΙΛ“Β…ζ≤ζΕ‘““œ©ΒΡ“άάΒΘ§”÷¥οΒΫΦθ…ΌCO2≈≈Ζ≈ΒΡΡΩΒΡΓΘ“‘Ρ…ΟΉΕΰ―θΜ·ν―ΡΛΈΣΙΛΉςΒγΦΪΘ§œΓΝρΥαΈΣΒγΫβ÷ »ή“ΚΘ§‘Ύ“ΜΕ®ΧθΦΰœ¬Ά®»κCO2Ϋχ––ΒγΫβΘ§‘Ύ“θΦΪΩ…÷ΤΒΟΒΆΟήΕ»Ψέ““œ©![]() Θ®Φρ≥ΤLDPEΘ©ΓΘ
Θ®Φρ≥ΤLDPEΘ©ΓΘ
ΔΌΒγΫβ ±Θ§“θΦΪΒΡΒγΦΪΖ¥”Π Ϋ «________ΓΘ
ΔΎΙΛ“Β…œ…ζ≤ζ1.4ΓΝ102kgΒΡLDPEΘ§άμ¬έ…œ–η“Σ±ξΉΦΉ¥Ωωœ¬________LΒΡCO2ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν– Β―ι≤ΌΉςΓΔœ÷œσΚΆΫα¬έΨυ’ΐ»ΖΒΡ «
―Γœν | Β―ι≤ΌΉς | Β―ιœ÷œσ | Β―ιΫα¬έ |
A | œρ | »ή“Κ≥»…Ϊ±δ…ν | ‘ω¥σ…ζ≥…Έο≈®Ε»Θ§ΤΫΚβ |
B | œρΫœ≈®ΒΡ |
|
|
C | »Γ | »ή“Κ÷–≥ωœ÷Ή©Κλ…Ϊ | ΒμΖέΆξ»ΪΥ°Ϋβ |
D | Ζ÷±πœρ | Φ”»κ | Ζ¥”ΠΈοΒΡ≈®Ε»‘Ϋ¥σΘ§Ζ¥”ΠΥΌ¬ ‘ΫΩλ |
A.AB.BC.CD.D
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Μ·―ß–Υ»Λ–ΓΉι‘Ύ Β―ι “ΧΫΨΩΙΐΕ…Ϋπ τ‘ΣΥΊΜ·ΚœΈοΒΡ–‘÷
(1)œρ![]() »ή“Κ÷–ΒΈΦ”NaOH»ή“ΚΘ§≤ζ…ζΑΉ…Ϊ≥ΝΒμΘ§ΒΪ―ΗΥΌ±δΈΣΜ“¬Χ…ΪΘ§Ήν÷’±δΈΣΚλΚ÷…ΪΘ§ΈΣΥ≥άϊΩ¥ΒΫΫœ≥Λ ±ΦδΒΡΑΉ…Ϊ≥ΝΒμΘ§…ηΦΤΝΥ»γΆΦΉΑ÷ΟΘΚΔΌΦλ≤ιΉΑ÷ΟΤχΟή–‘Θ§ΉΑ»κ“©ΤΖΘΜΔΎ¥ρΩΣ÷ΙΥ°Φ–KΘΜΔέ‘Ύ ‘Ιήb≥ωΩΎ ’Φ·ΤχΧε≤Δ―ι¥ΩΘΜΔήΙΊ±’÷ΙΥ°Φ–KΓΘ“‘…œ≤ΌΉς’ΐ»ΖΒΡΥ≥–ρ «ΘΚ________ΓΘ
»ή“Κ÷–ΒΈΦ”NaOH»ή“ΚΘ§≤ζ…ζΑΉ…Ϊ≥ΝΒμΘ§ΒΪ―ΗΥΌ±δΈΣΜ“¬Χ…ΪΘ§Ήν÷’±δΈΣΚλΚ÷…ΪΘ§ΈΣΥ≥άϊΩ¥ΒΫΫœ≥Λ ±ΦδΒΡΑΉ…Ϊ≥ΝΒμΘ§…ηΦΤΝΥ»γΆΦΉΑ÷ΟΘΚΔΌΦλ≤ιΉΑ÷ΟΤχΟή–‘Θ§ΉΑ»κ“©ΤΖΘΜΔΎ¥ρΩΣ÷ΙΥ°Φ–KΘΜΔέ‘Ύ ‘Ιήb≥ωΩΎ ’Φ·ΤχΧε≤Δ―ι¥ΩΘΜΔήΙΊ±’÷ΙΥ°Φ–KΓΘ“‘…œ≤ΌΉς’ΐ»ΖΒΡΥ≥–ρ «ΘΚ________ΓΘ
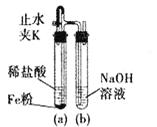
(2)Ρ≥ Β―ι–ΓΉι≥ΤΝΩ![]() ≤ίΥα―«ΧζΨßΧε
≤ίΥα―«ΧζΨßΧε![]() Φ”»»Ιΐ≥Χ÷–Θ§ΙΧΧε÷ ΝΩ±δΜ·»γΆΦΥυ ΨΘΚ
Φ”»»Ιΐ≥Χ÷–Θ§ΙΧΧε÷ ΝΩ±δΜ·»γΆΦΥυ ΨΘΚ
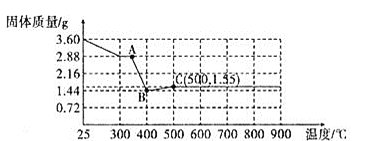
ΔΌ«κ–¥≥ωABΕΈΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ________________ΓΘ
ΔΎ![]() Βψ≥…Ζ÷ΈΣΘΚ________ΓΘ
Βψ≥…Ζ÷ΈΣΘΚ________ΓΘ
(3)œρ![]() »ή“Κ÷–Φ”»κΙΐΝΩ
»ή“Κ÷–Φ”»κΙΐΝΩ![]() »ή“ΚΘ§…ηΦΤ Β―ι÷ΛΟςΝΫ’ΏΖΔ…ζΝΥ―θΜ·ΜΙ‘≠Ζ¥”Π≤Δ«“ΈΣΩ…ΡφΖ¥”ΠΓΘ
»ή“ΚΘ§…ηΦΤ Β―ι÷ΛΟςΝΫ’ΏΖΔ…ζΝΥ―θΜ·ΜΙ‘≠Ζ¥”Π≤Δ«“ΈΣΩ…ΡφΖ¥”ΠΓΘ![]() Φρ“ΣΥΒΟς Β―ι≤Ϋ÷ηΓΔœ÷œσΚΆΫα¬έΘ§“«ΤςΚΆ“©ΤΖΉ‘―Γ
Φρ“ΣΥΒΟς Β―ι≤Ϋ÷ηΓΔœ÷œσΚΆΫα¬έΘ§“«ΤςΚΆ“©ΤΖΉ‘―Γ![]() ________________ΓΘ
________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΝζΩϊ»© «“Μ÷÷’δΙσœψΝœΘ§ΙψΖΚ”Π”Ο”ΎœψΝœΓΔ“Ϋ“©ΓΔ»ΨΝœΦΑ≈©“©––“ΒΓΘΤδΚœ≥…¬ΖœΏ»γΆΦΥυ Ψ(≤ΩΖ÷Ζ¥”Π≤ζΈοΚΆΖ¥”ΠΧθΦΰ“―¬‘»Ξ)ΘΚ

“―÷Σ”–ΜζΜ·―ßΖ¥”ΠΧθΦΰ≤ΜΆ§Θ§Ω……ζ≥…≤ΜΆ§ΒΡ≤ζΈοΘΚ
HX+CH3-CH=CH2 (XΈΣ¬±ΥΊ‘≠Ή”)
(XΈΣ¬±ΥΊ‘≠Ή”)
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©ΔΌΒΡΖ¥”Πάύ–ΆΈΣ___ΘΜD÷–ΒΡΚ§―θΙΌΡήΆ≈Οϊ≥Τ «___ΓΘ
Θ®2Θ©Ζ¥”ΠΔήΒΡΜ·―ßΖΫ≥Χ ΫΈΣ___ΓΘΖ¥”ΠΔίΒΡ ‘ΦΝ «___Θ§Ζ¥”ΠΧθΦΰ «___ΓΘ
Θ®3Θ©“―÷ΣAΈΣΜλΚœΈοΘ§…ηΦΤ≤Ϋ÷ηΔέΓΔΔήΒΡΡΩΒΡ «___ΓΘ
Θ®4Θ©ΝζΩϊ»©”κ–¬÷ΤCu(OH)2Ζ¥”Π≤ΔΥαΜ·ΚσΒΟΒΫEΘ§ΖϊΚœœ¬Ν–ΝΫΗωΧθΦΰΒΡEΒΡΆ§Ζ÷“λΙΙΧεΙ≤”–___÷÷ΓΘΔΌΡήΖΔ…ζ“χΨΒΖ¥”ΠΘ§“≤ΡήΖΔ…ζΥ°ΫβΖ¥”ΠΘΜΔΎ «±ΫΜΖΒΡΕΰ‘Σ»Γ¥ζ≤ζΈοΓΘ–¥≥ωΤδ÷–ΚΥ¥≈Ι≤’ώ«βΤΉ”–5÷÷Έϋ ’ΖεΒΡΈο÷ ΒΡΫαΙΙΦρ ΫΘΚ___ΓΘ
Θ®5Θ©≤Έ’’…œ ωΚœ≥…¬ΖœΏΘ§…ηΦΤ“‘2ΦΉΜυ1Θ§3ΕΓΕΰœ©ΈΣ‘≠ΝœΘ§Ψ≠»ΐ≤Ϋ÷Τ±Η2ΦΉΜυ1Θ§4ΕΓΕΰ»©( )ΒΡ¬ΖœΏΓΘ__
)ΒΡ¬ΖœΏΓΘ__
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ…ηNAΈΣΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΓΘœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
A.ΙΐΝΩΒΡΧζ‘Ύ1molCl2÷–»Μ…’Θ§Ήν÷’ΉΣ“ΤΒγΉ” ΐΈΣ2NA
B.‘Ύ50g÷ ΝΩΖ÷ ΐΈΣ46%ΒΡ““¥ΦΥ°»ή“Κ÷–Θ§Κ§«β‘≠Ή”Ήή ΐΈΣ6NA
C.5NH4NO3![]() 2HNO3ΘΪ4N2ΓϋΘΪ9H2OΖ¥”Π÷–Θ§…ζ≥…28gN2 ±Θ§ΉΣ“ΤΒΡΒγΉ” ΐΡΩΈΣ3.75NA
2HNO3ΘΪ4N2ΓϋΘΪ9H2OΖ¥”Π÷–Θ§…ζ≥…28gN2 ±Θ§ΉΣ“ΤΒΡΒγΉ” ΐΡΩΈΣ3.75NA
D.1L1mol/LNaCl»ή“ΚΚΆ1L1mol/LNaF»ή“Κ÷–άκΉ”Ήή ΐΘΚ«Α’Ώ–Γ”ΎΚσ’Ώ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“ΜΕ®Έ¬Ε»œ¬Θ§Ε‘”ΎΩ…ΡφΖ¥”ΠA(g)ΘΪ3B(g) ![]() 4C(g)ΒΡ–π ω÷–Θ§ΡήΥΒΟςΖ¥”Π“―¥οΒΫΤΫΚβΒΡ «(ΓΓΓΓ)
4C(g)ΒΡ–π ω÷–Θ§ΡήΥΒΟςΖ¥”Π“―¥οΒΫΤΫΚβΒΡ «(ΓΓΓΓ)
A.ΒΞΈΜ ±ΦδΡΎœϊΚΡ4a molΒΡCΆ§ ±Ζ÷Ϋβa mol AB.ΜλΚœΤχΧεΒΡΈο÷ ΒΡΝΩ≤Μ‘Ό±δΜ·
C.ΒΞΈΜ ±ΦδΡΎœϊΚΡ3a mol BΆ§ ±…ζ≥…4a mol CD.»ίΤςΡΎΒΡ―Ι«Ω≤Μ‘Ό±δΜ·
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–”–ΜζΈοΥΒΖ®≤Μ’ΐ»ΖΒΡ «Θ® Θ©
A. Ε‘ΦΉΜυ±Ϋ““œ©÷–ΉνΕύ”–17Ηω‘≠Ή”Ι≤Οφ
B. ίΝΜΖΘ®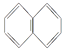 Θ©…œΒΡ“ΜΗωH‘≠Ή”±Μ-C4H9»Γ¥ζΚσΒΡ≤ζΈοΙ≤”–8÷÷
Θ©…œΒΡ“ΜΗωH‘≠Ή”±Μ-C4H9»Γ¥ζΚσΒΡ≤ζΈοΙ≤”–8÷÷
C. BrCH2CHBrCH2BrΒΡΟϊ≥ΤΈΣ»ΐδε±ϊΆι
D. ΝΔΖΫΆιΘ®![]() Θ©“Μ¬»¥ζΈο1÷÷ΓΔΕ଻¥ζΈο”–3÷÷ΓΔ»ΐ¬»¥ζΈο“≤”–3÷÷
Θ©“Μ¬»¥ζΈο1÷÷ΓΔΕ଻¥ζΈο”–3÷÷ΓΔ»ΐ¬»¥ζΈο“≤”–3÷÷
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com