
科目:高中化学 来源: 题型:解答题
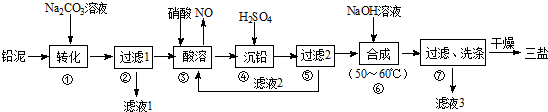
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0 mol/L | B. | 2.0 mol/L | C. | 3.0 mol/L | D. | 4.0 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学能转化为热能 | B. | 化学能转化为电能 | ||
| C. | 热能转化为化学能 | D. | 化学能转化为机械能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由H原子形成1 mol H-H键要吸收能量 | |
| B. | 所有燃烧的反应都是放热反应 | |
| C. | NaOH溶于水是放热反应 | |
| D. | 凡经加热而发生的化学反应都是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol Na被完全氧化生成Na2O2,失去2NA个电子 | |
| B. | 常温常压下,18 g H2O 中含有的原子总数为3NA | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA | |
| D. | 1 mol Cl2与1 mol Fe反应,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
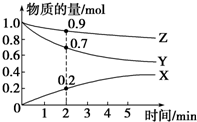 某温度时,在2L容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.由此分析,该反应的化学方程式为3Y+Z?2X;从反应开始至2min时,Z的反应速率为0.025mol•L-1•min-1.
某温度时,在2L容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.由此分析,该反应的化学方程式为3Y+Z?2X;从反应开始至2min时,Z的反应速率为0.025mol•L-1•min-1.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com