
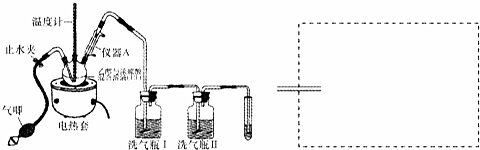
分析 (1)根据仪器的构造和常见仪器的名称进行分析;
(2)乙醇含有碳、氢、氧三种元素,浓硫酸具有脱水性,三颈瓶中温度逐渐升高,当温度达到100℃后,三颈瓶中溶液开始出现棕色,随后慢慢变成黑色,为碳单质,浓硫酸具有强的氧化性,产生刺激性气味气体为二氧化硫,浓硫酸与碳发生反应生成二氧化碳、二氧化硫和水;
(3)a.加成反应是有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应;
b.取代反应是有机物中的原子或原子团被其他的原子或原子团所代替生成新的化合物的反应;
c.消去反应是指在一定条件下,有机物脱去小分子生成分子中含有双键的不饱和有机物的反应;
d.物质与氧发生的化学反应叫氧化反应,或元素化合价升高的反应属于氧化反应;
(4)制取的乙烯气体中含有二氧化硫、二氧化碳等酸性气体,需用碱液吸收,洗气瓶Ⅱ中装有能与二氧化硫作用有显著特征的反应,证明酸性气体已被完全吸收,试管中装有高锰酸钾酸性溶液检验乙烯的生成;
(5)当高锰酸钾酸性溶液褪色时,通过试管部分的气体为乙烯,根据乙烯的物理性质选择收集装置;
(6)实验结束,停止加热,卸下乙烯收集装置;丙打开止水夹,挤压气唧,通过排气法将装置中剩余的二氧化硫压入吸收液中,防止污染空气.
解答 解:(1)装置中仪器A有进水出水的两个支管为冷凝装置,所以A为冷凝管,
故答案为:冷凝管;
(2)三颈瓶中温度逐渐升高,当温度达到100℃后,三颈瓶中溶液开始出现棕色,随后慢慢变成黑色,是因为浓硫酸具有脱水性,将乙醇中氢和氧按水的组成脱去,脱水生成碳单质,浓硫酸具有强氧化性,碳和浓硫酸反应生成二氧化碳、二氧化硫和水,反应的化学方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O,
故答案为:脱水;C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O;
(3)浓硫酸和乙醇的混合液(3:1)加热至140℃发生分子间脱水反应2C2H5OH$→_{140℃}^{浓硫酸}$C2H5OC2H5+H2O,生成乙醚,乙醇没有不饱和键,不属于加成反应,乙醚分子中无不饱和键,不属于消去反应,该反应无化合价变化,不属于氧化反应,两个乙醇分子反应,相当于一个乙醇分子中的一个氢原子被另一乙醇分子中乙基取代,属于取代反应,
故答案为:b;
(4)浓硫酸具有强氧化性,制取的乙烯气体中含有二氧化硫、二氧化碳等酸性气体,需用碱液吸收,可用盛有氢氧化钠的洗气瓶进行洗涤,二氧化硫能漂白品红,洗气瓶Ⅱ中装有能与二氧化硫作用有显著特征的反应,可用品红,证明酸性气体已被完全吸收,试管中装有高锰酸钾酸性溶液,乙烯能被高锰酸钾溶液氧化5CH2=CH2+12KMnO4+18H2SO4→10CO2+12MnSO4+28H2O+6K2SO4,导致高锰酸钾溶液褪色,试管中装有高锰酸钾酸性溶液检验乙烯的生成;
故答案为:NaOH;品红;证明二氧化硫已经完全被氢氧化钠溶液吸收,确保收集的气体是相对纯净的乙烯;
(5)当高锰酸钾酸性溶液褪色时,通过试管部分的气体为乙烯,乙烯的密度与空气接近,不能用排空气法收集,乙烯难溶于水,需用排水法收集,可用如下装置收集,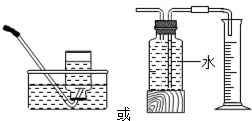 ,
,
故答案为: ;
;
(6)实验结束,停止加热,装置中剩余二氧化硫,二氧化硫为大气污染物,所以,卸下乙烯收集装置;丙打开止水夹,挤压气唧,通过排气法将装置中剩余的二氧化硫压入NaOH溶液中,被完全吸收,防止污染空气,
故答案为:将装置中剩余的二氧化硫排入NaOH溶液完全吸收,防止污染空气.
点评 本题考查了实验室制取乙烯,侧重考查副产物的性质和除杂,反应原理和题干条件的分析判断、信息应用是解题关键,题目难度中等.


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:选择题
| A. | 未用标准液润洗滴定管 | |
| B. | 盛标准液的滴定管尖嘴部分有气泡未排除就开始滴定 | |
| C. | 往锥形瓶中加待测液时,锥形瓶中有少许水 | |
| D. | 振荡时锥形瓶中液滴飞溅出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某密闭容器盛有0.1molN2和0.3molH2,充分反应后,形成的N-H键数目为0.6NA | |
| B. | 若由CO2和O2组成的混合物共有NA个分子,则其中所含的氧原子数为2NA | |
| C. | 常温下,1L0.1mol/LNH4NO3溶液中的氢原子数为0.4NA | |
| D. | 氢氧燃料电池正极消耗22.4L气体(标况下)时,电路中通过的电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾可做消毒剂 | |
| B. | 铝制品抛光车间须严格控制粉尘浓度以防爆炸 | |
| C. | 氧化铝可作耐火材料 | |
| D. | 金属铝无需经过特别处理就具有抗腐蚀能力 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
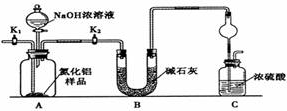
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | As的原子半径大于P,AsH3比PH3的热稳定性强 | |
| B. | P的非金属性强于Si,H3PO4比H2SiO3的酸性强 | |
| C. | Al2O3和MgO均可与NaOH溶液反应 | |
| D. | SO2和SO3混合气体通入Ba(NO3)2溶液可得到BaSO3和BaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
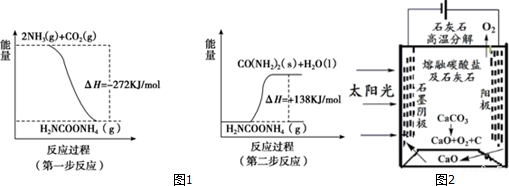
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 根据已学知识,请你回答下列问题:
根据已学知识,请你回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应/K/温度 | 458K 478K 488K |
| ① ② ③ | 1.78×104 1.43×104 1.29×104 1.91×107 1.58×107 1.45×107 8.11×108 3.12×108 2.00×108 |
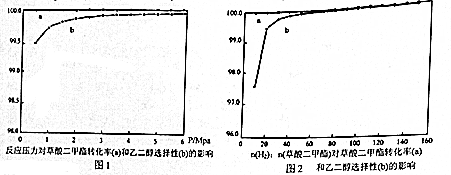
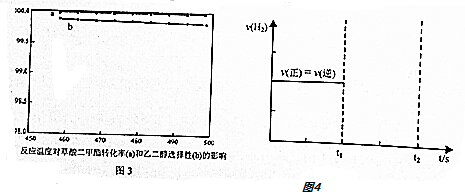
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com