
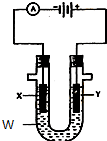
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液w;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液w;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:分析 (1)若X、Y都是惰性电极,W是饱和NaCl溶液,Y电极上氯离子放电生成氯气,X电极上氢离子放电,同时该电极附近生成氢氧根离子,电解氯化钠溶液得到氢氧化钠、氢气和氯气,根据电极反应式进行计算即可;
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,阳极应该是粗铜、阴极是纯铜,则X电极是纯铜、Y电极是粗铜,阴极上铜离子放电;
(3)若W仍然选用饱和NaCl溶液,X、Y分别是Fe、C棒,将X、Y用导线直接连接,和电源的正极相连的是阳极,电极上发生失电子的氧化反应,和电源的负极相连的是阴极,该电极上发生的是还原反应,据此回答.
解答 解:(1)①若w是饱和NaCl溶液,X、Y是惰性电极材料,Y是阳极,X是阴极,Y极上的电极反应式为:2Cl--2e-═Cl2↑;在X极上发生的反应是:2H++2e-=H2↑,该电极附近观察到的实验现象是冒出气泡,溶液变红,
故答案为:2Cl--2e-═Cl2↑;冒出气泡,溶液变红;
②电解饱和NaCl溶液总的离子反应方程式为2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH-;若电解过程中在两极生成22.4L即1mol气体(在标准况状下),所以得到氢气和氯气分别是0.1mol,转移电子是1mol,
故答案为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH-;1mol;
(2)①若要用电解方法精炼粗铜,电解质溶液W选用CuSO4溶液,则阴极材料是纯铜或精铜;该极上发生反应:Cu2++2e-═Cu;故答案为:纯铜或精铜;Cu2++2e-═Cu;
(3)W仍然选用饱和NaCl溶液,X、Y分别是Fe、C棒,将X、Y用导线直接连接,构成原电池,发生金属铁的吸氧腐蚀,则Y电极是正极;该电极上发生反应:O2+4e-+2H2O═4OH-.故答案为:正极;O2+4e-+2H2O═4OH-.
点评 本题考查原电池原理,为高频考点,侧重于学生的分析能力的考查,本题涉及电极反应式的书写、检验等知识点,知道离子放电顺序及电极反应式的书写方法,题目难度不大.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 它们都属于混合物 | B. | 它们都是乙烯的同系物 | ||
| C. | 它们的分子都不含氢原子 | D. | 聚四氟乙烯分子中含有双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中Na+浓度增大,有H2放出 | |
| B. | 溶液中Na+数目减少,有H2放出 | |
| C. | 溶液中Na+与OH-浓度都增大,有H2放出 | |
| D. | 溶液中OH-数目增大,有H2放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠溶于水中 | B. | CaCO3(S)分解为CaO(S)和CO2(g) | ||
| C. | 干冰的升华 | D. | NH3(g)和HCl(g)反应生成NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl | B. | KNO3 | C. | MgSO4 | D. | AlCl3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com