
【题目】经常有人因误食亚硝酸钠(NaNO2)而中毒。原因是NaNO2像食盐一样既有咸味,又有很强毒性。已知亚硝酸钠能发生如下反应:
2NaNO2+4HI=2NO+I2+2NaI+2H2O
(1)该反应的氧化剂是_______,被氧化的是_________元素。
(2)若此反应中电子转移数目为0.5mol,则被氧化的还原剂的物质的量为___________。
(3)用双线桥标出上述反应的电子转移的方向和数目。
科目:高中化学 来源: 题型:
【题目】N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g)![]() 4NO2(g)+O2(g) △H>0一定温度时,向密闭容器中通入N2O5,部分实验数据见下表:
4NO2(g)+O2(g) △H>0一定温度时,向密闭容器中通入N2O5,部分实验数据见下表:
时间/s[K] | 0 | 500 | 1000 | 1500 |
c(N2O5)/mol/L | 0.50 | 0.35 | 0.25 | 0.25 |
下列说法中错误的是
A.500 s时O2的浓度为0.075 mol/L
B.平衡后,升高温度,正反应速率先增大后减小
C.平衡后,要使平衡常数增大,改变的条件是升高温度
D.1000 s时将容器的体积缩小一半,重新达到平衡时0.25 mol/L<c(N2O5)<0.50 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸和盐酸组成的混合液100.0 mL,向其中加入氢氧化钡粉末4.275g,充分反应后,经过滤、洗涤、干燥,得到沉淀2.330g,同时测得滤液中的OH-离子浓度为0.100 mol·L-1 。(设溶液总体积始终不变)请列式计算
(1)原溶液中硫酸的物质的量为____________。
(2)原混合液中盐酸的物质的量浓度_______________。
(3)若将原硫酸和盐酸混合溶液100ml与足量金属锌反应,则在标况下产生的气体体积为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与纯水的电离相似,液氨中也存在着微弱的电离:2NH3![]() NH4++NH2-据此判断以下叙述中错误的是( )
NH4++NH2-据此判断以下叙述中错误的是( )
A. NH3、NH4+、NH2-的电子数相等,化学性质也相同
B. 一定温度下,液氨中c(NH4+)·c(NH2-)是一个常数
C. 液氨的电离达到平衡时c(NH3)≠c(NH4+)=c(NH2-)
D. 加入其他物质,液氨中c(NH4+)与c(NH2-)的比值可能不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制下列溶液时常需加入少量括号内的物质,其中不是为了抑制离子水解的是
A.FeSO4(Fe) B.SnCl2(HCl) C.FeCl3(HCl) D.NaAlO2(NaOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为 1L的密闭容器中充入1mol CO和2mol H2混合气体,发生以下反应:CO(g)+2H2(g)![]() CH3OH(g)。T1、T2温度下,CH3OH的物质的量随着时间的变化关系如下图所示。下列有关说法正确的是
CH3OH(g)。T1、T2温度下,CH3OH的物质的量随着时间的变化关系如下图所示。下列有关说法正确的是

A.T1>T2
B.K(T1)>K(T2)
C.T1温度下达到平衡后,再充入一定量CO,CO的转化率增大
D.T2温度下,0~10min间v(H2)=0.06mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对初中化学知识的总结,错误的是
A.化学基本反应类型包括化合反应、分解反应、置换反应和复分解反应四种
B.六大基本营养素是蛋白质、糖类、油脂、维生素、无机盐和水
C.由同种元素组成的物质一定是纯净物
D.遇到火灾时,用湿毛巾捂住口鼻,匍匐逃离火灾现场
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
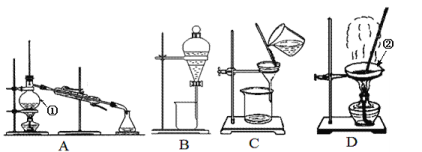
(1)装置A中仪器①的名称是_____________,装置D中仪器②的名称是_____________。
(2)从氯化钾溶液中得到氯化钾固体,应选择装置___________(填代表装置图的字母,下同);从碘水中分离出I2,选择装置__________,该装置的主要仪器名称是_________。分离饱和食盐水与沙子的混合物,应选择装置__________,分离四氯化碳(沸点为76.75℃)和甲苯(110.6℃)的混合物,应选择装置__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学键的叙述正确的是( )
A.所有化学物质内部都存在化学键
B.共价键存在于原子之间,也存在于分子之间
C.离子键是阴、阳离子之间的相互吸引力
D.化学键通常指的是相邻的两个或多个原子间的强烈的相互作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com