
工业废气中氮氧化合物是造成污染的主要来源.为治污,工业上通常通入NH3与之发生下列反应:NOX+NH3→N2+H2O.现有NO、NO2的混合气3L,可用同温同压下的3.5LNH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比( )
|
| A. | 1:3 | B. | 2:1 | C. | 1:1 | D. | 1:4 |
| 氮的氧化物的性质及其对环境的影响;有关混合物反应的计算.. | |
| 专题: | 守恒法. |
| 分析: | 氮氧化物与氨气发生的反应是氧化还原反应,氮氧化物把氨气氧化为氮气,本身被还原为氮气,可以利用反应方程式通过设未知列方程组计算;也可以根据氧化还原反应的电子守恒计算;也可以利用平均值法计算, |
| 解答: | 解:根据反应可知:氨气被氧化为氮气,NH3~N2~3e﹣;一氧化氮被还原为氮气,NO~N2~2e﹣二氧化氮被还原为氮气 NO2~N2~4e﹣设一氧化氮体积为x,二氧化氮体积为3﹣x,氨气的体积为3.5L,根据电子守恒可知:3.5L×3=2x+4×(3﹣x), x=0.75L,二氧化氮体积为2.25L,则相同条件下,混合气体中NO和NO2的体积比等于物质的量之比=0.75:2.25=1:3; 故选A. |
| 点评: | 本题考查了氮氧化物的污染与防治,氧化还原反应的电子守恒,混合物的计算. |


科目:高中化学 来源: 题型:
已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO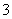 +H2O
+H2O H2SO3+OH-①
H2SO3+OH-①
HSO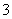
 H++SO
H++SO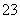 ②
②
向0.1 mol·L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是 ( )
A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO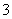 )增大
)增大
B.加入少量Na2SO3固体,则c(H+)+c(Na+)=c(HSO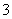 )+c(OH-)+
)+c(OH-)+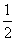 c(SO
c(SO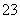 )
)
C.加入少量NaOH溶液,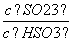 、
、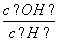 的值均增大
的值均增大
D.加入氨水至中性,则2c(Na+)=c(SO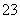 )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
有一包固体粉末,由CaCO3、Na2SO4、KNO3、BaCl2、CuSO4中的三种物质组成,取样品进行如下实验:
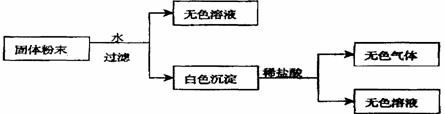
从实验可以判断,该固体粉末中(1)一定不含有 ,
(2)它的组成可能是 或 。
(3)加入盐酸后发生反应的离子方程式为 。
(4)要进一步确定其组成还应进行的实验操作是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在一容积可变的容器中,反应2A(g)+B(g)⇌2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol.保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡左移的是( )
|
| A. | 均减半 | B. | 均加倍 | C. | 均增加1mol | D. | 均减少1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解一定浓度的硫酸铜溶液,长时间通电后,向所得溶液中加入0.2mol Cu(OH)2恰好恢复到电解前的浓度和pH.则电解过程中转移电子的总物质的量为( )
|
| A. | 0.2mol | B. | 0.4mol | C. | 0.6mol | D. | 0.8mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知可逆反应:M(g)+N(g)⇌P(g)+Q(g)△H>0,请回答下列问题.
(1)在某温度下,反应物的起始浓度分别为:c(M)=1mol•L﹣1,c(N)=2.4mol•L﹣1,达到平衡后,M的转化率为60%,此时N的转化率为 .
(2)若反应温度升高,M的转化率 (填“增大”、“减小”或“不变”)
(3)若反应温度不变,反应物的起始浓度分别为c(M)=4mol•L﹣1,c(N)=amol•L﹣1;达到平衡后,c(P)=2mol•L﹣1,a= .
(4)若反应温度不变,反应物的起始浓度为:c(M)=c(N)=b mol•L﹣1,达到平衡后,M的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
|
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的杀菌净化 |
|
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
|
| C. | MgO的熔点很高,可用于制作耐高温材料 |
|
| D. | 电解MgCl2饱和溶液,可制得金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写中,正确的是( )。
A.氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu
B.稀硫酸与铁粉反应:2Fe+6H+=2Fe3++3H2↑
C.氢氧化钡溶液与稀硫酸反应:Ba2++SO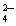 =BaSO4↓
=BaSO4↓
D.碳酸钙与盐酸反应: +2H+=H2O+CO2↑
+2H+=H2O+CO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com