
����Ŀ������ѧ����ѡ��5���л���ѧ������
ijҩ���ںϳ�һ����������ѪС��ۼ���ҩ��ʱʹ�õ��м����л���M����ͼΪ�л���M��![]() ���ĺϳ�·�ߣ�
���ĺϳ�·�ߣ�
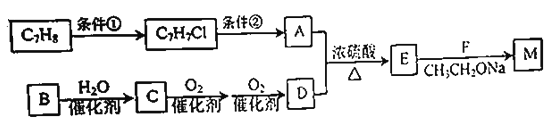
��֪����B��ʯ���ѽ����Ҫ�����������ں���������չ��ˮƽ��
��R��CHO+R�@��CH2COOR ![]()
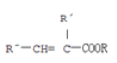
�ش��������⣺
��1��E�Ļ�ѧ������___________��C�Ĺ���������Ϊ____________��
��2����Ӧ������Ϊ_____________��
��3��C7H7C1��A�Ļ�ѧ����ʽΪ____________________��
A+D��E�ķ�Ӧ����Ϊ________________��
��4��F���ӵĽṹ��ʽΪ________���������______��ԭ�ӹ�ƽ�档
��5����ͬʱ��������������M��ͬ���칹�干��______�֡������������칹��
�����ڱ��Ķ�λ��ȡ�����������M������ͬ�����ţ��� �뱽�����������ܹ�����ˮ�ⷴӦ���ܹ�����������Ӧ��
�뱽�����������ܹ�����ˮ�ⷴӦ���ܹ�����������Ӧ��
��6�����������ϳ�·�ߣ�����д�����еĿհף�������Ʊ��۱�ϩ������ĺϳ�·�ߡ�______

���𰸡� ���ᱽ���� �ǻ� Cl2������ ![]() ȡ����Ӧ��������Ӧ��
ȡ����Ӧ��������Ӧ�� ![]() 11 8
11 8 
��������������������м���M�ϳ�·��Ϊ���У��ص㿼���л�����������л���Ӧԭ����д��������л���Ӧ���������������ơ�ԭ�ӹ��桢�л��ϳ�·����ơ��ڶ���֪���̵ķ����У��������Ʒ����л����̷����е�Ӧ�á�
����������Ӧ�����Ʒ���M�ĺϳ�·�߽��з���������M�Ľṹ����֪���ķ�Ӧԭ�������Եõ��ϳ�M��ԭ��Ϊ![]() ��
��![]() ������֪����֪BΪCH2=CH2����CΪCH3CH2OH����һ����������CH3CHO�����������ɵ�DΪ���ᣬA����7��Cԭ�ӣ�����EΪ
������֪����֪BΪCH2=CH2����CΪCH3CH2OH����һ����������CH3CHO�����������ɵ�DΪ���ᣬA����7��Cԭ�ӣ�����EΪ![]() ��FΪ
��FΪ![]() �����Կ�ͼ��C7H8Ϊ
�����Կ�ͼ��C7H8Ϊ![]() ��C7H7ClΪ
��C7H7ClΪ![]() ����1��E�������뱽�״��γɵ���������Ϊ���ᱽ������C���Ҵ������������ǻ����𰸣����ᱽ�״����ǻ�����2����Ӧ���Ǽױ��ϼ�һ��Hԭ�ӱ�Clȡ������Ӧ������Cl2�����ա��𰸣�Cl2�����ա���3��A�DZ��״���
����1��E�������뱽�״��γɵ���������Ϊ���ᱽ������C���Ҵ������������ǻ����𰸣����ᱽ�״����ǻ�����2����Ӧ���Ǽױ��ϼ�һ��Hԭ�ӱ�Clȡ������Ӧ������Cl2�����ա��𰸣�Cl2�����ա���3��A�DZ��״���![]() ��NaOH��Һ�м���ʱ��Clԭ�ӱ��ǻ�ȡ�����ɱ��״���NaCl��A��D��Ӧ����Ҫ�仯���ǻ����Ȼ���Ӧ��������ˮ������������Ӧ��ȡ����Ӧ����ȷ�𰸣�
��NaOH��Һ�м���ʱ��Clԭ�ӱ��ǻ�ȡ�����ɱ��״���NaCl��A��D��Ӧ����Ҫ�仯���ǻ����Ȼ���Ӧ��������ˮ������������Ӧ��ȡ����Ӧ����ȷ�𰸣�![]() ��������Ӧ����ȡ����Ӧ������4��FΪ
��������Ӧ����ȡ����Ӧ������4��FΪ![]() ����������ϩ�ṹ����6��ԭ�ӹ��棬��F����Ԫ����ֱ�����ӵ�3��Hԭ�ӡ�һ��Cԭ�ӹ��棬�Ը�Cԭ��Ϊ�������ȩ����3��ԭ�ӹ����ҿ�������Ԫ�����棬���Ը÷����е�����11��ԭ�ӿ��ܴ���ͬһƽ�档�𰸣�
����������ϩ�ṹ����6��ԭ�ӹ��棬��F����Ԫ����ֱ�����ӵ�3��Hԭ�ӡ�һ��Cԭ�ӹ��棬�Ը�Cԭ��Ϊ�������ȩ����3��ԭ�ӹ����ҿ�������Ԫ�����棬���Ը÷����е�����11��ԭ�ӿ��ܴ���ͬһƽ�档�𰸣�![]() ��11����5��M�ķ���ʽΪC14H12O3�������Ͷ�Ϊ(14��2+2-12)/2=9����֪�٢�˵�������ṹΪ
��11����5��M�ķ���ʽΪC14H12O3�������Ͷ�Ϊ(14��2+2-12)/2=9����֪�٢�˵�������ṹΪ![]() ���һ�����1��C=C��һ����COO�����������ǹ�4��Cԭ�ӡ�����ˮ��˵����������������˵�����ӽṹ�к���ȩ������ȩ��ֻ����������ϴ��ڣ�������COO��ΪHCOOC���ṹ�������ӳ�����A����Ϊ����CH=CHCH2OOCH����CH2CH=CHOOCH����(CH3)C=CHOOCH����CH=C(CH3)OOCH��
���һ�����1��C=C��һ����COO�����������ǹ�4��Cԭ�ӡ�����ˮ��˵����������������˵�����ӽṹ�к���ȩ������ȩ��ֻ����������ϴ��ڣ�������COO��ΪHCOOC���ṹ�������ӳ�����A����Ϊ����CH=CHCH2OOCH����CH2CH=CHOOCH����(CH3)C=CHOOCH����CH=C(CH3)OOCH��![]() ��
��![]() ��
��![]() ��
��![]() ��8�֡��𰸣�8����6������֪�������ж�ͼ�����Ҵ��������·�Ӧ�ķ�Ӧ��Ӧ��Ϊȩ��������ͼ���·�Ϊ����������Ϸ�Ϊ��ȩ�����߷�Ӧ����CH2=CHCOOCH3���پ����Ӿ۷�Ӧ�õ����ղ��CH3OHת���HCHO�ķ�Ӧ��������Cu�������������������½��д��������״�������������Ӧ������Ũ���ᣬ���ȡ��𰸣�
��8�֡��𰸣�8����6������֪�������ж�ͼ�����Ҵ��������·�Ӧ�ķ�Ӧ��Ӧ��Ϊȩ��������ͼ���·�Ϊ����������Ϸ�Ϊ��ȩ�����߷�Ӧ����CH2=CHCOOCH3���پ����Ӿ۷�Ӧ�õ����ղ��CH3OHת���HCHO�ķ�Ӧ��������Cu�������������������½��д��������״�������������Ӧ������Ũ���ᣬ���ȡ��𰸣�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ֽ�2molA��1molB����2L�ܱ������з�����Ӧ��2A(g)+B(g) ![]() 2C(g)���ֱ���Tl��T2ʱ���������C�����ʵ�����ʱ��仯��ͼ��ʾ������˵����ȷ����
2C(g)���ֱ���Tl��T2ʱ���������C�����ʵ�����ʱ��仯��ͼ��ʾ������˵����ȷ����

A. T1<T2
B. �÷�Ӧ���¶�ΪT1ʱ�ﵽƽ��ʱ��������A��C�����ʵ���Ũ�����
C. �¶�ΪT2ʱ��2s��B��ƽ������Ϊ0.3mol��L-1��s-l
D. �¶�ΪT1ʱ����ƽ��ʱ��Ӧ��A��ת����Ϊ60%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ھ����ܱ������з�����Ӧ��aM(g)+bN(g) ![]() cW(g) ��ƽ����M�����Ũ��Ϊ0.5mol/L�������ܱ��������������1�����ٴ�ƽ��ʱ�����M�����Ũ��Ϊ0.3mol/L��������������ȷ����
cW(g) ��ƽ����M�����Ũ��Ϊ0.5mol/L�������ܱ��������������1�����ٴ�ƽ��ʱ�����M�����Ũ��Ϊ0.3mol/L��������������ȷ����
A����Ӧ�������� B��ƽ�������ƶ�
C����ϵ�¶����� D��W��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2013��7��23������������,����ʡ�ϳ��ؿƼ����¡����������ʯ��ҵ����ء�1 molʯī��һ����������ȫת��Ϊ���ʯ,�������仯��ͼ��ʾ,��E1=393.5 kJ,��E2=395.4 kJ,����˵����ȷ���ǣ� ��
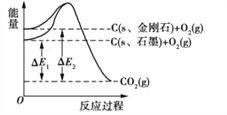
A. 1 molʯī��ȫת��Ϊ���ʯ������1.9 kJ������
B. ʯīת��Ϊ���ʯ���������仯
C. ���ʯ���ȶ���ǿ��ʯī��
D. 1 mol���ʯ����������1mol CO2������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ҵ�ϳɰ�ʱ���ϳ�����ÿ����1molNH3���ų�46.1kJ��������
ijС���о���500���¸÷�Ӧ�����е������仯�����Ƿֱ��������ΪVL���������º����ܱ������м���һ�����ķ�Ӧ�ʹ������ͬ�¶��·�����Ӧ������������£�
���� | ��ʼʱ���������ʵ���/mol | �ﵽƽ���ʱ�� | ��ƽ��ʱ��ϵ�����ı仯/kJ | ||
N2 | H2 | NH3 | |||
a | 1 | 4 | 0 | t1min | �ų�������36.88kJ |
b | 2 | 8 | 0 | t2min | �ų�������Q |
������a�У�0~t1ʱ���ƽ����Ӧ����Ϊ��(H2)=___________��
������������ȷ����________������ĸ��ţ���
A������b�з�Ӧ��ƽ��״̬ʱ��Q��73.76kJ
B��ƽ��ʱ����������H2������������
C����Ӧ��ʼʱ���������з�Ӧ�Ļ�ѧ��Ӧ�������
D��ƽ��ʱ��������N2��ת���ʣ�a<b
��2����Ϊԭ�ϣ��ϳ����صķ�Ӧԭ��Ϊ��2NH3(g)��CO2(g)![]() CO(NH2)2(l)��H2O(g) ��H=akJ��mol-1��
CO(NH2)2(l)��H2O(g) ��H=akJ��mol-1��
Ϊ�о�ƽ��ʱCO2��ת�����뷴Ӧ��Ͷ�ϱ�[![]() ]���¶ȵĹ�ϵ���о�С����10L�����ܱ������н���ģ�ⷴӦ���������߷ֱ��ʾ�ڲ�ͬͶ�ϱ�ʱ��CO2��ת�������¶�֮��Ĺ�ϵ����
]���¶ȵĹ�ϵ���о�С����10L�����ܱ������н���ģ�ⷴӦ���������߷ֱ��ʾ�ڲ�ͬͶ�ϱ�ʱ��CO2��ת�������¶�֮��Ĺ�ϵ����
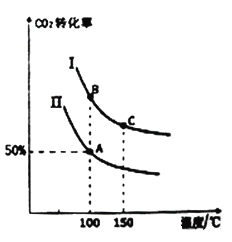
��a_______0(���������)��
����n(CO2)��ʼ=10mol�����ߢ��Ͷ�ϱ�Ϊ0.4����100�������·�����Ӧ����ƽ����A�㣬��A������ʼѹǿ��Ϊ_______��
��A��ƽ�ⳣ����B��ƽ�ⳣ����Ĺ�ϵ��KA_______KB(�������������)��
��3�����ð������������������ȡ����N2H4����ͼ���ɡ��������������γɵ���ɫȼ�ϵ�أ���ʯīΪ�缫�ĵ�ع���ԭ��ʾ��ͼ��b�缫Ϊ_______�����������������д���õ�ع���ʱa�缫�ĵ缫��Ӧʽ_______��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʹ�õ�ȼ��Ҫ����������Ϊ��̬����һ��ѹ���ͱ��Һ����һ��ѹ(����)����������ȼ�ա��±��е��л����ܽϺõ�������ЩҪ�����(����)
ѡ�� | A | B | C | D |
����ʽ | C2H6 | C3H8 | C4H10 | C5H12 |
�۵�/�� | ��183.3 | ��181.7 | ��138.4 | ��127.9 |
�е�/�� | ��88.6 | ��42.1 | ��0.5 | 36.1 |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����շۣ�Na2S2O4���м�ǿ�Ļ�ԭ�ԣ�����ˮ��ʪ������ֽⷢ�ȣ����ڼ��Ի����½��ȶ����ش��������⣺
(1)����������Ʊ�
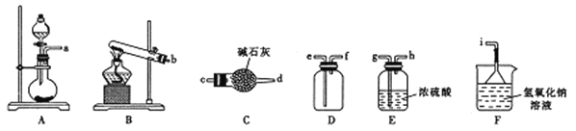
����������ķ���װ�ÿ���ѡ����ͼ�е�_____________�����д��ĸ������Ӧ�Ļ�ѧ����ʽΪ______________________��
�����ռ�һƿ����Ķ�������ѡ����ͼ�е�װ�ã���ӿڵ�����˳��Ϊ����װ����__________________����______��______�� ____________����������������Сд��ĸ��ʾ��
(2)���շ۵��Ʊ�
��35-45���£���SO2����ͨ��п��һˮ����Һ�У���ͼ����ʹ֮������Ӧ����ZnS2O4������Ӧ��ȫ�����ߺ���ˮԡװ�ò���ȴ�����£���������ƿ�м���18%��NaOH��Һ��ʹ֮������Ӧ����Na2S2O4��Zn(OH)2����һϵ�в�����õ���ˮNa2S2O4��Ʒ��
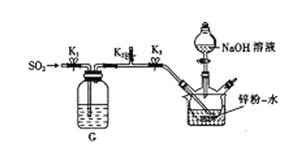
��ʵ�鿪ʼʱ��Ӧ�ȹر�ֹˮ��K3����K1��K2��ͨ��һ��ʱ��SO2����ԭ����__________��
��ͨ���۲�_________________������ֹˮ��K1������SO2�����١�
����ZnS2O4����Na2S2O4�Ļ�ѧ����ʽΪ_____________��
(3)��ȡ2.0gNa2S2O4��Ʒ������ˮ�У����100mL����Һ��ȡ��10mL����Һ���Թ��У���0 .10 mol/L��KMnO4��Һ�ζ����ζ����յ�ʱ����ΪNa2SO4��MnSO4�����ظ���������2�Σ�ƽ��������Һ12.00mL�������Ʒ��Na2S2O4����������Ϊ_______�����ʲ����뷴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Խ��������Ʒ��Խ�õ���(����)
A. CH3(CH2)6CH3
B. CH3CH(CH3)CH2CH2CH3
C. (CH3)2CHCH2C(CH3)3
D. CH3(CH2)14CH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Σ�3PbO��PbSO4��H2O��������������ϩ�����ȶ�����200�����Ͽ�ʼʧȥ�ᾧˮ��������ˮ���л��ܼ�����200.0tǦ�ࣨ��Ҫ�ɷ�ΪPbO��Pb��PbSO4�ȣ�Ϊԭ���Ʊ����εĹ���������ͼ��ʾ��

��֪��PbSO4��PbCO3���ܽ�Ⱥ��ܶȻ�Ksp���±���
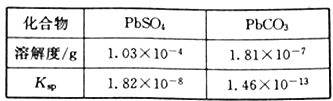
��1�������ת����Ŀ����_______����Һ1�е�����ΪNa2CO3��_______���ѧʽ����
��2�����������ʱ��Ϊ����������ʣ��ɲ�ȡ�Ĵ�ʩ��_________����дһ����������Ǧ�����ᷴӦ����Pb(NO3)2��NO�����ӷ���ʽΪ__________________��
��3����Һ2�п�ѭ�����õ����ʵĻ�ѧʽΪ_______��������ܳ�Ǧ�����Һ��c(Pb2+)=1.82��10-5mol/L�����ʱc(SO42-)=______mol/L��
��4�������ϴ�Ӳ���ʱ����������Ƿ�ϴ����ȫ�ķ�����________________��
��5������ϳ����εĻ�ѧ����ʽΪ____________�����õ��������������99.Ot������Ǧ���е�ǦԪ����80��ת��Ϊ���Σ���Ǧ����ǦԪ�ص���������Ϊ________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com