


| 0.25×0.25 |
| 0.52×1.04 |
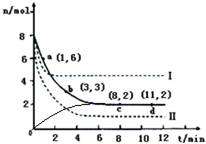 ,故答案为:
,故答案为: ;
;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 项目 | 结论 |
| A | 丙烯、氯乙烯、苯 | 分子内所有原子均共面 |
| B | 由溴丙烷制丙醇;由丙烯制丙醇 | 属同种反应类型 |
| C | 乙烯和苯加入溴水中,水层褪色 | 褪色原理相同 |
| D | C4H9Cl的同分异构体数目(不考虑立体异构) | 共4种 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )
元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )| A、D在过量的B中燃烧的主要产物为DB3 |
| B、C的氢化物的水溶液酸性比E的强 |
| C、D与B形成的阴离子可能有DB32-、D2B42- |
| D、E单质中由于形成了氢键,所以很容易液化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1种 | B、2种 | C、3种 | D、4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、臭氧可用于水体消毒,是因为臭氧能杀死水中的细菌 |
| B、明矾能水解生成氢氧化铝胶体,可用做净水剂 |
| C、食盐中添加碘酸钾,是因为碘酸钾具有氧化性 |
| D、禁止使用四乙基铅作汽油抗暴震剂,可减少汽车尾气污染 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com