
在不同温度下,水达到电离平衡时c(H+)与c(OH-)的关系如图所示,下列说法中正确的是

A.100 ℃时,pH=12的NaOH溶液和pH=2的H2SO4溶液等体积混合时恰好中和,所得溶液的pH等于7
B.25 ℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl溶液等体积混合,所得溶液的pH等于7
C.25 ℃时,0.2 mol/L NaOH溶液与0.2 mol/L醋酸等体积混合后恰好中和,所得溶液pH等于7
D.25 ℃时,pH=12的氨水和pH=2的H2SO4溶液等体积混合,所得溶液的pH大于7
科目:高中化学 来源:2016届河北省高三上学期第四次月考化学试卷(解析版) 题型:选择题
在BaSO4饱和溶液中加入少量的BaCl2溶液,产生BaSO4沉淀,若以Ksp表 示BaSO4的溶度积常数,则平衡后溶液中
示BaSO4的溶度积常数,则平衡后溶液中
A.c(Ba2+)=c(SO42-)=(Ksp)1/2
B.c(Ba2+)·c(SO42-)>Ksp,c(Ba2+)=c(SO42-)
C.c(Ba2+)·c(SO42-)=Ksp,c(Ba2+)>c(SO42-)
D.c(Ba2+)·c(SO42-)≠Ksp,c(Ba2+)<c(SO42-)
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上学期第二次精英对抗赛化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列说法不正确的是
A.煤、石油、天然气是不可再生能源,风能、生物质能、沼气是可再生能源
B.“84消毒液”具有强氧化性,可做环境的消毒剂从而预防流感
C.已知水热反应是指在高温高压下,将二氧化碳转化为有机物的技术,则水热反应可以降低自然界中碳的含量
D.已知PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为“细颗粒物”,则PM2.5在空气中有可能形成胶体
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期12月月考化学试卷(解析版) 题型:选择题
下列实验装置设计正确、且能达到目的的是
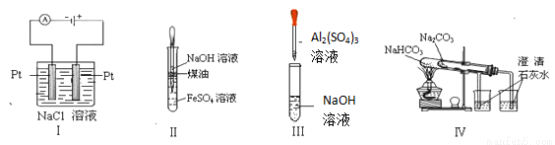
A.实验Ⅰ:制取金属钠
B.实验II:制取Fe(OH)2
C.实验Ⅲ:制取少量的氢氧化铝
D.实验Ⅳ:比较两种物质的热稳定性
查看答案和解析>>
科目:高中化学 来源:2016届广东省等三校高三上学期12月联考理综化学试卷(解析版) 题型:选择题
利用右图所示装置进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:Cl > C > Si | |
B | 稀硫酸 | Na2S | AgNO3与AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
C | 浓氨水 | 碱石灰 | AlCl3溶液 | Al(OH)3是两性氢氧化物 | |
D | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 |
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第四次月考化学试卷(解析版) 题型:选择题
下列电解质溶液的有关叙述正确的是
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
C.含1 mol KOH的溶液与1 mol CO2完全反应后,溶液中c(K+)= c(HCO3-)
D.在CH3COONa溶液中加入适量CH3COOH,可使 c(Na+)= c(CH3COO-)
c(Na+)= c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2016届河南省洛阳市高三上学期12月统考化学试卷(解析版) 题型:选择题
心脏起搏器一般是给心跳缓慢的病人使用。某种类型的心脏起搏器工作时发生下列反应:4Li+2SOC12 =4LiC1+S+SO2,下列有关判断正确的是
A.还原剂只有锂
B.SOC12中每个原子都达到8电子稳定结构
C.氧化产物包括LiCl和SO2
D.生成1. 12 LSO2时,反应转移电子为0.2 mol
查看答案和解析>>
科目:高中化学 来源:2016届山东省北校高三上学期第二次单元测试化学试卷(解析版) 题型:选择题
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是

A.温度: T1>T2>T3
B.正反应速率:υ(b)>υ(d) υ(a)>υ(c)
C.平衡常数:K(a)>K(c) K(b)=K(d)
D.平均摩尔质量: M(b)>M(d) M(a)<M(c)
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三上学期第四次质检化学试卷(解析版) 题型:填空题
某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B = H++HB-,HB- 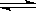 H++B2-
H++B2-
回答下列问题:
(1)Na2B溶液显 (填“酸性”“中性”或“碱性”),理由是 。(用离子方程式表示)
(2)在0.1 mol·L-1 Na2B溶液中,下列粒子浓度关系式正确的是 。
A.c(Na+)+(OH-)=c(H+)+c(HB-)
B.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-)
C.c(Na+)=2c(B2-)+2c(HB-)
D. c(B2-)+ c(HB-)=0.1mol·L-1
(3)已知0.1 mol·L-1 NaHB溶液的pH=2,则0.1mol·L-1 H2B溶液中氢离子的物质的量浓度可能是 0.11 mol·L-1(填“<”“>”或”=”),理由是 。
(4)0.1 mol·L-1 NaHB溶液中各种离子浓度由大到小的顺序是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com