
| A、FeCl2 |
| B、F2 |
| C、Al2O3 |
| D、C |
| ||


科目:高中化学 来源: 题型:
| A、18gNH+4中含有的电子数为10NA |
| B、78gNa2O2固体中含有的阴离子数为2NA |
| C、1L0.1 mol/L醋酸溶液中含有的氢离子数为0.1NA |
| D、标准状况下,2.24L苯含有分子的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol?L-1) | 0.64 | 0.5 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 试管 | 温度 | 过氧化氢浓度 | 催化剂 |
| A | 室温(25℃) | 12% | 有 |
| B | 水浴加热(50℃) | 4% | 无 |
| C | 水浴加热(50℃) | 12% | 有 |
| D | 室温( 25℃) | 4% | 无 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:

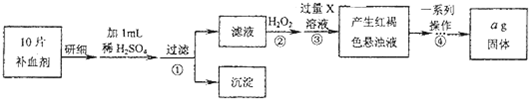
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


 (R表示烃基,R′和R″表示烃基或氢)
(R表示烃基,R′和R″表示烃基或氢) 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| n(CO2) |
| n(SO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯酚中滴加少量的稀溴水出现了三溴苯酚的白色沉淀 |
| B、检验C2H5Cl中氯原子时,将C2H5Cl和NaOH溶液混合加热后,加入稀硫酸进行酸化 |
| C、用无水乙醇和浓H2SO4共热至140℃可以制得乙烯气体 |
| D、制取溴苯应用液溴、铁屑和苯混合,反应后并用稀碱液洗涤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com