
 周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增。R的基态原子中占据哑铃形原子轨道的电子数为1;W的氢化物的沸点比同族其它元素氢化物的沸点高;X2 +与W2-具有相同的电子层结构;Y元素原子的3P能级处于半充满状态;Z+的电子层都充满电子。请回答下列问题:
周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增。R的基态原子中占据哑铃形原子轨道的电子数为1;W的氢化物的沸点比同族其它元素氢化物的沸点高;X2 +与W2-具有相同的电子层结构;Y元素原子的3P能级处于半充满状态;Z+的电子层都充满电子。请回答下列问题:
(1)写出Z的基态原子外围电子排布_______________________。
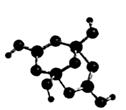
(2)R的某种钠盐晶体,其阴离子Am- (含R、W、氢三种元素)的球棍模型如上图所示:在Am-中,R原子轨道杂化类型有____________;m=____________。(填数字)
(3)经X射线探明,X与W形成化合物的晶体结构与NaCl的晶体结构相似,X2+的配位原子所构成的立体几何构型为______________________。
(4)往Z的硫酸盐溶液中加入过量氨水,可生成[Z(NH3)4]SO4,下列说法正确的是______________________。
A.[Z(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.在[Z(NH3)4]2+中Z2+给出孤对电子,NH3提供空轨道
C.[Z(NH3)4]SO4组成元素中第一电离能最大的是氧元素
D.SO42-与PO43-互为等电子体,空间构型均为四面体
(5)固体YCl5的结构实际上是YCl4+和YCl6-构成的离子晶体,其晶体结构与CsCl相似。若晶胞边长为a pm,则晶胞的密度为___________________________g•cm-3。(已知阿伏伽德罗常数为NA,用含a和NA的代数式表示)
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
用NA表示阿伏德罗常数,下列叙述一定正确的是( )
A.标准状况下,2.24LH2O含有的质子数为 NA
B.等物质的量的氮气和氧气,都含有2NA个原子
C.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组,为了探究过氧化钠的强氧化性,设计了如图的实验装置。
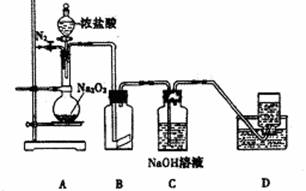
实验步骤及现象如下:
①检查装置气密性后,装人药品并连接仪器:
②缓慢通人一定量的N2后,将装置D连接好(导管末端未伸人集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,反应剧烈,产生黄绿色气体。
③一段时间后,将导管末端伸人集气瓶中收集气体。装置D中收集到能使带火星的木条复燃的无色气体。
④反应结束后,关闭分液漏斗的活塞,再通人一定量的N2,至装置中气体无色。
(1) 装置B中的湿润的红色纸条褪色,证明A中反应有_______(填化学式)生成。若B中改放湿润的淀粉KI试纸,仅凭试纸变蓝的现象不能证明上述结论,请用离子方程式说明原因____________________________________________
(2) 装置C的作用是______________________________________________
(3) 甲同学认为O2是 Na2O2被盐酸中的HCl还原所得。乙同学认为此结论不正确,他可能的理由为①____________________________________;②______________________________
(4) 实验证明,Na2O2与干燥的HCl能反应,得到Cl2,请写出该的化学方程式:
_____________________________________________________;
该反应一般不用于实验室快速制取纯净的Cl2,理由是________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
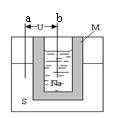
下图为钠硫高能电池的结构示意图,M为Na2O和Al2O3的混合物,电池反应为2Na+xS Na2Sx该电池的工作温度为320℃左右,下列说法错误的是
Na2Sx该电池的工作温度为320℃左右,下列说法错误的是
A.a为电池正极,b为电池负极
B.电池放电时,正极反应为xS+2e- = Sx2-
C.电池充电时,Na所在电极连接电源正极
D.M的作用为导电和隔离钠和硫
查看答案和解析>>
科目:高中化学 来源: 题型:
已知钠放置于空气中可发生如下变化:
Na Na2O
Na2O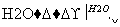 NaOH
NaOH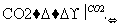 Na2CO3·10H2O
Na2CO3·10H2O
根据此变化回答以下问题:
(1)请写出①②步转化的化学方程式:
①_________________________________________________________;
②_________________________________________________________。
(2)已知钠在空气中燃烧可生成一种淡黄色物质,该物质可与CO2、H2O发生反应,根据以上叙述回答:
①该淡黄色物质的化学式为________;
②该淡黄色物质与CO2、H2O反应的化学方程式为
______________________________________________________________,
_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)。
Ⅰ.(1)能证明氯水具有漂白性的是________(填“a”、“b”、“c”或“d”)。
(2)c过程中的现象是_____________________________________________,
b过程中反应的化学方程式为______________________________。
(3)久置的氯水变为________,用化学反应方程式表示为_______________。
(4)实验室保存饱和氯水的方法是_________________________________。
Ⅱ.用滴管将新制的饱和氯水慢慢滴入含酚酞的NaOH稀溶液中。当滴到最后一滴时红色突然退去。试回答下列问题:
(1)是由于_________________________________________________;
(2)是由于________________________________________________。
简述怎样用实验证明红色退去的原因是(1)还是(2):
_____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com