
| t1��t2 | t2��t3 | t3��t4 | t4��t5 | t5��t6 |
| K1 | K2 | K3 | K4 | K5 |
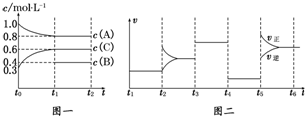
���� ��1������v=$\frac{��c}{��t}$����v��C����
��2����3��ͼ���������ֲ�ͬ�����Ӱ�컯ѧ��ƽ�⣬��Ӱ��ƽ��������У�Ũ�ȡ��¶ȡ�ѹǿ��������
t3��t4��t4��t5������ƽ���Dz��ƶ��ģ���ֻ����ѹǿ�ʹ���Ӱ��ģ����Ӧ���ƶϸ÷�ӦΪ������仯�ķ�Ӧ��
t3��t4��ƽ���ԭƽ�������Ҫ�죬��t4��t5�������ֱ�������ǰ��Ӧ�ǼӴ�������Ϊ����ֻ����һ�Σ�t4��t5��Ϊ��ѹ��
��Ӧ���Ũ�Ƚ��ͣ��������Ũ�������ͼһ��֪��AΪ��Ӧ�CΪ�����A�ı仯Ϊ0.2mol/L��C�ı仯��Ϊ0.3mol/L�������ڸ÷�ӦΪ������仯�ķ�Ӧ������BΪ��Ӧ����ݻ�ѧ��Ӧ������֮�ȵ��ڻ�ѧ����ʽǰ�ļ���ϵ���ȣ�д���÷�Ӧ�ķ���ʽΪ2A��g��+B��g��?3C��g������ʼ2molA����Ӧ��Ũ��Ϊ1mol/L�������Ӧ��2L��
t5-t6 ��Ϊ�����¶ȣ�v�����������棩��ƽ��������Ӧ�����ƶ��������¶�ƽ�������ȷ����ƶ���
����ƽ�ⳣ����ƽ���ƶ����K1��K2��K3��K4��K5֮��Ĺ�ϵ��
��4��Ҫ�ﵽt1ʱ��ͬ����ƽ�⣬ӦΪ��ȫ��Чƽ�⣬���������ԭƽ����ȣ�
��� �⣺��1��15min�ڣ���CŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊv��C��=$\frac{0.6mol/L-0.3mol/L}{15min}$=0.02 mol/��L•min����
�ʴ�Ϊ��0.02 mol/��L•min����
��2��t3��t4��t4��t5������ƽ���Dz��ƶ��ģ���ֻ����ѹǿ�ʹ���Ӱ��ģ����Ӧ���ƶϸ÷�ӦΪ������仯�ķ�Ӧ��
t3��t4��ƽ���ԭƽ�������Ҫ�죬��t4��t5�������ֱ�������ǰ��Ӧ�ǼӴ�������Ϊ����ֻ����һ�Σ�t4��t5��Ϊ��ѹ��
��Ӧ���Ũ�Ƚ��ͣ��������Ũ�������ͼһ��֪��AΪ��Ӧ�CΪ�����A�ı仯Ϊ0.2mol/L��C�ı仯��Ϊ0.3mol/L�������ڸ÷�ӦΪ������仯�ķ�Ӧ������BΪ��Ӧ����ݻ�ѧ��Ӧ������֮�ȵ��ڻ�ѧ����ʽǰ�ļ���ϵ���ȣ��÷�Ӧ�ķ���ʽΪ2A��g��+B��g��?3C��g�������ԣ���c��B��=$\frac{1}{2}$��n��A��=$\frac{1}{2}$��0.2mol/L=0.1mol/L����ʼ2molA����Ӧ��Ũ��Ϊ1mol/L�������Ӧ��$\frac{2mol}{1mol/L}$=2L����B����ʼ���ʵ���Ϊn��B��=��0.1mol/L+0.4mol/L����2L=1mol��
t1-t2�Σ�����ƽ��״̬��c��A��ƽ��=0.8mol/L��c��B��ƽ��=0.4mol/L��c��C��ƽ��=0.6mol/L��
K1=$\frac{{c}^{3}��C��}{{c}^{2}��A��•c��B��}$=$\frac{0��{6}^{3}}{0��{8}^{2}��0.4}$=0.84��t2-t3�Σ�Ϊ�ı�Ũ�ȣ�ƽ���ƶ���ƽ�ⳣ�����䣬K2=0.84��
t3-t4�Σ�ʹ�ô������ӿ췴Ӧ��ƽ�ⳣ�����䣬K3=0.84��
t4-t5�Σ�Ϊ����ѹǿ����Ӧ���ʽ��ͣ�ƽ�ⲻ�ƶ���ƽ�ⳣ�����䣬K4=0.84��
t5-t6�Σ�Ϊ�����¶ȣ�ƽ��������Ӧ�����ƶ���ƽ�ⳣ������
�� K1=K2=K3=K4��K5��
�ʴ�Ϊ����Сѹǿ��1.0mol�� 0.84��K1=K2=K3=K4��K5��
��3�����ݷ���ʽ���㣬��A�����ʵ������仯��0.01mol�����˹����������������Ƚ�������Ϊa kJ����Ӧ2molAʱ����������200akJ������ͼ���֪��t5��t6��ӦΪ�����¶ȣ�����Ӧ���ʴ����淴Ӧ���ʣ�ƽ��������Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ�������Ȼ�ѧ����ʽΪ2A��g��+B��g��?3C��g����H=+200a kJ/mol��
�ʴ�Ϊ��2A��g��+B��g��?3C��g����H=+200a kJ/mol��
��4����Ӧ�ķ���ʽΪ2A��g��+B��g��?3C��g����
���ݷ���ʽ���㣬��ʼʱ����C��������ת��ΪA��B��
��A�����ʵ���Ϊ2mol+$\frac{2}{3}$��0.6mol=2.4mol��B�����ʵ���Ϊ1mol+$\frac{1}{3}$��0.6mol=1.2mol��
����ͬ�����£�����ʼʱ�����м���a mol A��b mol B��c mol C��Ҫ�ﵽt1ʱ��ͬ����ƽ�⣬���������ʵ����ʵ��������������ԭƽ����ȣ�
������a+$\frac{2}{3}$c=2.4��b+$\frac{1}{3}$c=1.2��
�ʴ�Ϊ��a+$\frac{2}{3}$c=2.4��b+$\frac{1}{3}$c=1.2��
���� ������ͼ�����ʽ����Ӱ�컯ѧ��Ӧ�����Լ���ѧƽ���ƶ������أ���Ŀ�Ѷ��еȣ�ע���Чƽ�����⣬Ϊ������ѵ㣬Ҳ���״��㣮


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | PH=10��Mg��OH��2��ҺC��Mg2+��=10-8 mol•L-1 ����֪Mg��OH��2KSP=1��10-16�� | |
| B�� | ��֪AgClKSP=1.8��10-10��Ag2CrO4KSP=1.2��10-12��AgCl���ܽ��һ����Ag2CrO4�� | |
| C�� | �ڱ���AgCl��Һ�м���NaI���岻�ᷢ���仯 | |
| D�� | Fe3+��������Һ��һ����������Fe��OH��3���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
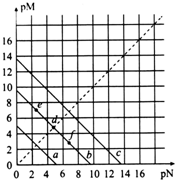 ��֪��T��ʱ��Ksp��CaSO4��=4.90��10-5��Ksp��CaCO3��=2.8��10-9��Ksp��PbCO3��=8.4��10-14�������εij����ܽ�ƽ��������ͼ��ʾ��pM=-lgc�������ӣ���pN=-lgc�������ӣ�������˵����ȷ���ǣ�������
��֪��T��ʱ��Ksp��CaSO4��=4.90��10-5��Ksp��CaCO3��=2.8��10-9��Ksp��PbCO3��=8.4��10-14�������εij����ܽ�ƽ��������ͼ��ʾ��pM=-lgc�������ӣ���pN=-lgc�������ӣ�������˵����ȷ���ǣ�������| A�� | a�ߴ�������PbCO3 | |
| B�� | T��ʱ����10 mLˮ�м���CaCO3��PbCO3�����߾����ͣ���Һ��c��Ca2+����c��Pb2+��=3��10-5 | |
| C�� | T��ʱ����CaSO4�����м���1 mol/L��Na2CO3��Һ��CaSO4������ת��ΪCaCO3���� | |
| D�� | T��ʱ����CaCO3����Һ�м���NH4Cl���壬��ʹͼ����d����f��ת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��Ӧ2Mg��s��+CO2��g��=C��s��+2MgO��s�����Է����У���÷�Ӧ�ġ�H��0 | |
| B�� | Ϊ������������ĺڰߣ�Ag2S�������������������������ʳ��ˮ�в������Ӵ� | |
| C�� | �����£���ϡCH3COONa��Һ��ˮϡ�ͺ���Һ��n��H+��•n��OH-������ | |
| D�� | ��ʢ��Ca��OH��2����Һ�ľ����ܱ������У�����������CaO��ĩ����Һ��Ca2+��Ŀ���䣬pH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | +5 | B�� | +4 | C�� | +3 | D�� | +2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
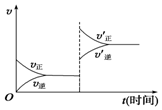 ���ڴﵽƽ��Ŀ��淴Ӧ��X+Y?W+Z������ѹǿ�������淴Ӧ���ʣ�v���ı仯��ͼ��ʾ��������֪X��Y��Z��W�ľۼ�״̬�����ǣ�������
���ڴﵽƽ��Ŀ��淴Ӧ��X+Y?W+Z������ѹǿ�������淴Ӧ���ʣ�v���ı仯��ͼ��ʾ��������֪X��Y��Z��W�ľۼ�״̬�����ǣ�������| A�� | Z��WΪ���壬X��Y��֮һΪ���� | B�� | Z��W��֮һΪ���壬X��YΪ������ | ||
| C�� | X��Y��Z��Ϊ���壬WΪ������ | D�� | X��Y��Z��W��Ϊ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com