
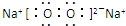 写出B的氢化物的结构式:
写出B的氢化物的结构式: 用电子式表示A、C两元素形成AC2的过程:
用电子式表示A、C两元素形成AC2的过程: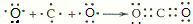
分析 A、B、C、D、E五种短周期元素.原子序数依次增大,C的阴离子和D的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体甲,则C为O元素、D为Na元素,甲为过氧化钠;A原子的最外层上有4个电子,原子序数小于C,则A为C元素;B的原子序数介于A、C之间,所以B为N元素,E的L层电子数等于K、M两个电子层上的电子数之和,则D原子M层电子数为8-2=6,核外各层电子分别为2、8、6,则E为S元素,据此答题.
解答 解:A、B、C、D、E五种短周期元素.原子序数依次增大,C的阴离子和D的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体甲,则C为O元素、D为Na元素,甲为过氧化钠;A原子的最外层上有4个电子,原子序数小于C,则A为C元素;B的原子序数介于A、C之间,所以B为N元素,E的L层电子数等于K、M两个电子层上的电子数之和,则D原子M层电子数为8-2=6,核外各层电子分别为2、8、6,则E为S元素,
(1)根据上面的分析可知,B为N元素,B元素的名称氮,
故答案为:氮:
(2)E为S元素,E在周期表中的位置是第三周期第ⅥA族,
故答案为:第三周期第ⅥA族;
(3)D为Na元素,D的质子数比中子数少1,则D的质量数为23,D的原子符号为2311Na,
故答案为:2311Na;
(4)甲为过氧化钠,甲的电子式为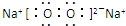 ,B为N元素,B的氢化物为氨气,氨气的结构式为
,B为N元素,B的氢化物为氨气,氨气的结构式为 ,A为C元素,C为O元素,A、C两元素形成的化合物为CO2,用电子式表示CO2形成的过程为:
,A为C元素,C为O元素,A、C两元素形成的化合物为CO2,用电子式表示CO2形成的过程为: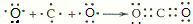 ,
,
故答案为: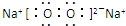 ;
; ;
;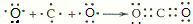 ;
;
(5)甲为过氧化钠,A为C元素,甲和A的最高价氧化物即二氧化碳,二氧化碳与过氧化钠反应生成碳酸钠与氧气,化学反应方程式为:2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2.
点评 本题考查结构性质位置关系应用,侧重对化学用语的考查,比较基础,注意对基础知识的积累掌握.


科目:高中化学 来源: 题型:解答题
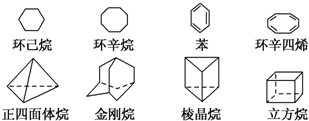 如图是八种环状的烃类物质:
如图是八种环状的烃类物质: 1,4-二甲苯、
1,4-二甲苯、 1,3,5-三甲苯.
1,3,5-三甲苯.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ | B. | K+、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$ | ||
| C. | Na+、K+、SO${\;}_{3}^{2-}$ | D. | Na+、NO${\;}_{3}^{-}$、SO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
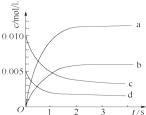 在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间变化如表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式相同的不同物质一定是同分异构体 | |
| B. | 通式相同的不同物质一定属于同系物 | |
| C. | 相对分子质量相同的不同物质一定是同分异构体 | |
| D. | 分子式相同,元素的质量分数也相同的物质是同种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH可能等于7 | |
| B. | c(HCO3- )=c(CH3COO-) | |
| C. | c(OH-)=$\frac{c(C{H}_{3}COOH)Kw}{c(C{H}_{3}CO{O}^{-})Ka}$ | |
| D. | c(HCO3- )+c(H2CO3)+c(CO3 2-)=c(CH3COOH)+c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
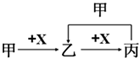
| A. | 甲为C,X为O2 | B. | 甲为Fe,X为Cl2 | ||
| C. | 甲为SO2,X为NaOH溶液 | D. | 甲为Fe,X为稀硝酸溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com