
| A. | 31.3 g | B. | 27.9 g | C. | 25.6 g | D. | 19.8 g |
分析 Zn与Fe的混合物在一定量的稀HNO3溶液中完全溶解,往溶液中滴加KSCN后,溶液不变色,说明生成硝酸锌、硝酸亚铁,硝酸完全反应,且收集到标准状况下4.48L无色但遇空气变红色的气体为NO,则向反应后的溶液中加入足量的氨水(不考虑沉淀在氨水中溶解损失),在空气中不断搅拌,充分反应后,由于氢氧化亚铁易被氧化,故最终生成沉淀为Zn(OH)2、Fe(OH)3,根据Zn与Fe总质量、电子转移守恒计算二者各自物质的量,再根据电荷守恒计算沉淀中氢氧根离子物质的量,沉淀质量=金属质量+沉淀中氢氧根离子质量.
解答 解:Zn与Fe的混合物在一定量的稀HNO3溶液中完全溶解,往溶液中滴加KSCN后,溶液不变色,说明生成硝酸锌、硝酸亚铁,硝酸完全反应,且收集到标准状况下4.48L无色但遇空气变红色的气体为NO,其物质的量为$\frac{4.48L}{22.4L/mol}$=0.2mol,
设Zn、Fe的物质的量分别为xmol、ymol,根据Zn与Fe总质量、电子转移守恒,可得:
$\left\{\begin{array}{l}{65x+56y=17.7}\\{2x+2y=0.2×(5-2)}\end{array}\right.$
解得x=0.1、y=0.2
则向反应后的溶液中加入足量的氨水(不考虑沉淀在氨水中溶解损失),在空气中不断搅拌,充分反应后,由于氢氧化亚铁易被氧化,故最终生成沉淀为Zn(OH)2、Fe(OH)3,根据电荷守恒可知沉淀中氢氧根离子物质的量=0.1mol×2+0.2mol×3=0.8mol,故沉淀质量=17.7g+0.8mol×17g/mol=31.3g,
故选:A.
点评 本题考查混合物有关计算,侧重考查学生分析计算能力,注意利用守恒法进行解答,难度中等.


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:实验题
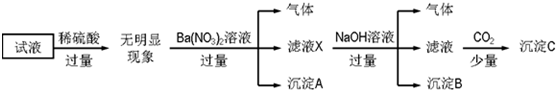
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该反应为缩聚反应 | |
| B. | PPV是聚苯乙炔 | |
| C. | PPV与聚苯乙烯的最小结构单元组成相同 | |
| D. | 1 mol  最多可与2 mol H2发生反应 最多可与2 mol H2发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
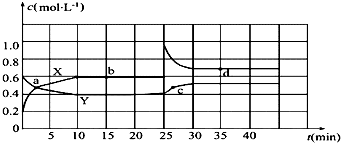
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
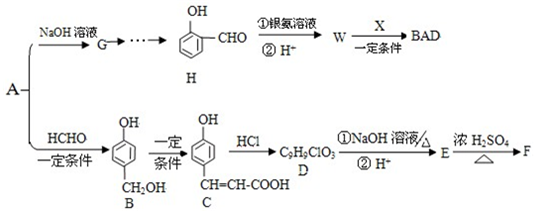


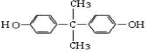 ,推测B的核磁共振氢谱中显示有5种不同化学环境的氢原子.
,推测B的核磁共振氢谱中显示有5种不同化学环境的氢原子.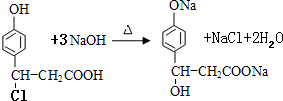 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
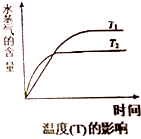 研究表明,在CuZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
研究表明,在CuZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:| T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 543 | Cat.1 | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.1 | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
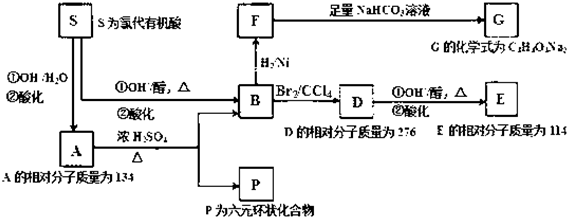
 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
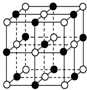 已知尿素(结构简式:
已知尿素(结构简式: )可用于制有机铁肥三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.回答下列问题.
)可用于制有机铁肥三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com