
分析 ①依据氧化铝为两性氧化性与氢氧化钠反应身材偏铝酸钠和水,可知氧化锌与氢氧化钠溶液反应生成偏铝酸锌和水;
②尿素[CO(NH2)2]和次氯酸钠、氢氧化钠溶液反应生成联氨、碳酸钠、水,依据原子个数守恒和氧化还原反应规律可知还有另一种钠盐为氯化钠.
解答 解:①氧化锌与氢氧化钠溶液反应生成偏铝酸锌和水,离子方程式:ZnO+2OH-═ZnO22-+H2O;
故答案为:ZnO+2OH-═ZnO22-+H2O;
②尿素[CO(NH2)2]和次氯酸钠、氢氧化钠溶液反应生成联氨、碳酸钠、水、氯化钠,化学方程式:CO(NH2)2+NaClO+2NaOH$\frac{\underline{\;KMnO_{4}\;}}{\;}$N2H4+Na2CO3+NaCl+H2O;
故答案为:CO(NH2)2+NaClO+2NaOH$\frac{\underline{\;KMnO_{4}\;}}{\;}$N2H4+Na2CO3+NaCl+H2O.
点评 本题考查了化学方程式、离子方程式的书写,明确反应实质及物质的性质是解题关键,注意氧化还原反应规律,题目难度中等.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 25℃时向水中加入少量固体CH3COONa,平衡逆向移动,c (H+)降低,Kw不变 | |
| B. | 由水电离出的c(H+)=10-12mol•L-1的溶液中:Na+、Ba2+、HCO3-、Cl-可以大量共存 | |
| C. | 向Na2CO3溶液中加入NaOH溶液后,c(CO32- )减少 | |
| D. | 某温度时的混合溶液中c(H+)=$\sqrt{{K}_{W}}$mol•L-1,说明该溶液呈中性(KW为该温度时水的离子积常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的水与重水含有的中子数 | |
| B. | 等质量的O2和O3含有的原子数 | |
| C. | 同温、同压同体积的CO和NO含有的质子数 | |
| D. | 等物质的量的铁分别与足量氯气和硫完全反应时转移的电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

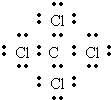 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 带相反电荷离子之间的静电作用称为离子键 | |
| B. | 金属元素与非金属元素化合时,不一定形成离子键 | |
| C. | 某元素的原子最外层只有一个电子,它跟卤素结合时所形成的化学键不一定是离子键 | |
| D. | 非金属元素形成的化合物中不可能含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲醇发生氧化反应 | |
| B. | O2在电极上得电子,被还原 | |
| C. | 电池工作时,甲醇电极反应式:CH3OH-6e-+H2O=CO2↑+6H+ | |
| D. | 该电池的甲醇燃料并没有储存在电池内部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com