

| △c |
| △t |
| 2.25mol/L |
| 10min |


科目:高中化学 来源: 题型:
 右图是某中学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )
右图是某中学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )| A、该硫酸试剂的物质的量浓度为18.4 mol?L-1 |
| B、该硫酸与等体积的水混合所得溶液的质量分数小于49% |
| C、50mL该H2SO4中加入足量的铜片并加热,被还原的H2SO4的物质的量为0.46mol |
| D、常温下2.7 gAl与足量的该硫酸反应可得到标准状况下的H2 3.36 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Zn+2HCl=ZnCl2+H2↑ | ||||
| B、Na2CO3+CaCl2=CaCO3↓+2NaCl | ||||
C、2H2O
| ||||
| D、H2+Cl2=2HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
 CO和H2的混合气体俗称合成气,是一种重要的工业原料气,可以在一定条件下制备甲醇,二甲醚等多种有机物.工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.
CO和H2的混合气体俗称合成气,是一种重要的工业原料气,可以在一定条件下制备甲醇,二甲醚等多种有机物.工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.| 时间/min 物质 浓度 |
0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2mol?L-1 | 0.13mol?L-1 | 0.1mol?L-1 | 0.1mol?L-1 | 0.09mol?L-1 |
| H2 | 0mol?L-1 | 0.2mol?L-1 | 0.3mol?L-1 | 0.3mol?L-1 | 0.33mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 设nA为阿伏加德罗常数的值,下列叙述正确的是( )
设nA为阿伏加德罗常数的值,下列叙述正确的是( )| A、常温常压下,16g14CH4所含中子数目为8nA |
| B、标准状况下,22.4 LCCl4所含分子数目为nA |
| C、1 L 0.5 mol?L-1的CH3COONa溶液中所含的CH3COO-离子数目为0.5nA |
| D、6.2g白磷(分子式为P4,分子结构如图所示)所含P-键数目为0.3nA |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
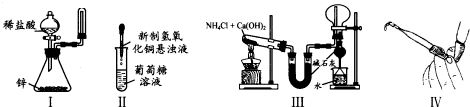
| A、实验I:制取并收集氢气 |
| B、实验II:验证葡萄糖的还原性 |
| C、实验III:实验室制氨气并收集干燥的氨气 |
| D、实验Ⅳ:检查碱式滴定管是否漏液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molNa2O2和水完全反应,转移电子数为2nA |
| B、0.5L0.2mol?L-1FeCl3溶液中,含Fe3+离子数为0.1nA |
| C、理论上氢氧燃料电池负极消耗11.2L标准状况下气体,外线路通过电子数为nA |
| D、常温常压下,28g乙烯和丙烯混合气体含有的碳原子总数为2.5nA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1moL铁与足量氯气完全反应转移的电子数目为2NA |
| B、32g氧气和32g臭氧(O3)所含有的氧原子数均为2NA |
| C、100mLlmol/LFeCl3溶液中含有Fe3+为0.1NA |
| D、用含4molHCl的浓盐酸与足量MnO2加热反应,产生Cl2的分子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com