
��4�֣�ʵ��������250 mL 1.0 mol��L��1 H2SO4��Һ���ش��������⣺
��1����Ҫ18 mol��L��1 H2SO4��Һ�������________mL��
��2��Ӧѡ������______������Ͳ��ȡŨ���ᡣ
A��10 mL B��25 mL C��50 mL D��100 mL
��3��ijͬѧ������ƿ������Һ����ˮʱ���������˿̶��ߣ���(��)��ˮ����һЩ�����¼�ˮ���̶��ߡ���������ʹ������Һ��Ũ��________(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��
��4��ijͬѧ��������ƿ��ת��Һ��ʱ��δ������ˮϴ���ձ�����������ʹ������Һ��Ũ��________(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��
13.9�� B��ƫ�ͣ�ƫ��
��������
�����������1����Һϡ��ǰ����Һ�����ʵ����ʵ������ֲ��䣬����Ҫ18mol?L-1 H2SO4��Һ���ܶ�Ϊ1.84g�Mcm3���������V����18mol?L-1?VL=0.25L?1.0mol?L-1�����V��0.0139L=13.9mL����2����Һ�����Ϊ13.9mL��ѡ������ӽ�����Ͳ����25mL�ģ�ѡB����3����ˮʱ���������˿̶��ߣ��Ὣ��Һϡ�ͣ���������ʹ������Һ��Ũ��ƫ�ͣ���4��������ƿ��ת��Һ��ʱ��δ������ˮϴ���ձ�����һ�������ʻ�մ���ձ��ϣ�������Һ��Ũ��ƫ�͡�
���㣺����һ�����ʵ���Ũ����Һ�����ơ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡУ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
(8��)����ͬ�¶Ⱥ���ͬѹǿ״���£���ͬ�����CO��CO2�У����������ݣ�
��1��������������ԭ����Ŀ֮��Ϊ
��2�����ǵ�����֮��Ϊ
��3�����ǵ��ܶ�֮��Ϊ
��4�����������ĵ�����֮��Ϊ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ʵ����
��14�֣��к�����ָ�������кͷ�Ӧ����lmol H2O���ų���������ijѧ����ͨ���ⶨ��Ӧ���������ų��������������к��ȡ�����50mL0.5mol/L��������50mL0.55mol/L��NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ����ش��������⣺

��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ��______���ձ���������������ĭ��������______��
��2�����ձ����粻��Ӳֽ�壬����õ��к�����ֵ_________(�ƫ����ƫС��������Ӱ�족)
��3��ʵ���и���60 mL 0.50 mol/L�������50mL 0.55 mol/L��NaOH��Һ����Ӧ��������ʵ����ȣ����ų�������________(���ȡ�����ȡ�������________________�������к��ȵ���ֵ��________(���ȡ�����ȡ�)��������_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪H��H����Ϊ436 KJ/mol��H��N����Ϊ391KJ/mol�����ݻ�ѧ����ʽ��N2( g ) + 3H2( g ) = 2NH3( g ) ��H=��92.4 KJ/mol����N��N���ļ�����
A��431 KJ/mol B��946 KJ/mol C��649 KJ/mol D��869 KJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A���Ȼ�ѧ����ʽ�У���ѧʽǰ��Ļ�ѧ�������ȿɱ�ʾ�������ֿɱ�ʾ���ʵ�����
B���Ȼ�ѧ����ʽ�У����û��ע���¶Ⱥ�ѹǿ�����ʾ�ڱ�״���²�õ����ݡ�
C����д�Ȼ�ѧ����ʽʱ������Ҫд����Ӧ�ȵķ��ź���ֵ����Ҫע�������ʵľۼ�״̬��
D�����ǻ��Ϸ�Ӧ���Ƿ��ȷ�Ӧ���ֽⷴӦ�������ȷ�Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ȥ�����еģ�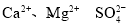 ����ɳ���ɽ���������ˮ��Ȼ������������������
����ɳ���ɽ���������ˮ��Ȼ������������������
�ٹ��ˣ��ڼӹ���������������Һ���ۼ�����������ܼӹ�����̼������Һ���ݼӹ������Ȼ�����Һ��
������ȷ�IJ���˳����
A���ڢݢܢ٢� B���٢ܢڢݢ�
C���ݢڢ٢ܢ� D���ܢ٢ڢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������һƿ�����Ǽ��ҵĻ�����֪���ҵ�ijЩ�������±���ʾ��
���� | �۵� | �е� | �ܶ� | ˮ���ܽ��� |
�� | �C98�� | 57��7�� | 0��93g�� | ���� |
�� | �C84�� | 77�� | 0��90g�� | ���� |
�ݴˣ������һ���������ѷ�����
A����ȡ�� B�����˷� C������ D����Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡУ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
X��Y��Z�������壬��a mol X��b mol Y����һ�ܱ������У�������ӦX��2Y 2Z.�ﵽƽ��ʱ�������ǵ����ʵ������㣺n(X)��n(Y)��n(Z)����Y��ת����Ϊ
2Z.�ﵽƽ��ʱ�������ǵ����ʵ������㣺n(X)��n(Y)��n(Z)����Y��ת����Ϊ
A��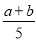 ��100% B��
��100% B��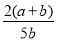 ��100%
��100%
C��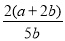 ��100% D��
��100% D��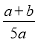 ��100%
��100%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
AB��CD��EF��Ϊ1��1�����ӻ�����������������ж����ǵ��۵��ɸ����͵�˳����
AB | CD | EF | |
���ӵ���� | 1 | 1 | 2 |
����(10��10 m) | 2��31 | 3��18 | 2��10 |
A��CD��AB��EF B�� AB��EF��CD
C��AB��CD��EF D��EF��AB��CD
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com