
����Ŀ����¼Ƭ�����ڹʹ������չʾ��ר�Ҿ�տ�ļ��պͶԴ�ͳ�Ļ����Ȱ�����أ�Ҳ������ᵽ��ѧ���������ﱣ���еľ����á�
��.ij����������������Ĺ������£�
(1)�����ʴ��ijɷ֡�
��ʴ����Ҫ�ɷֵĻ�ѧʽ | |||
Fe3O4 | Fe2O3��H2O | FeO(OH) | FeOCl |
FeOCl����Ԫ�صĻ��ϼ�Ϊ_______��
(2)��ѧ�����������ȡ���ԭ���γ�Fe3O4�����㡣(��֪��Cl����ӿ����ĸ�ʴ)
�����̣���������û��ʢ��0.5 mol��L-1 Na2SO3��0.5 mol��L-1 NaOH��Һ�������У�����������60��90�棬һ��ʱ���ȡ�������NaOH��Һϴ������Cl����
�����ȷ�Ӧ��FeOCl + OH�� = FeO(OH) + Cl�������ӷ�Ӧ����������Ũ�ȼ�С�ķ�����еģ�����ͬ�¶��£�FeOCl��FeO(OH)���ܽ�ȣ�s(FeOCl)______s[FeO(OH)](�������)��
�ڻ�ԭ��Ӧ��Na2SO3��ԭFeO(OH)�γ�Fe3O4����ƽ��ѧ����ʽ��
___Na2SO3 + ___FeO(OH) = ___Na2SO4 + ___Fe3O4 + ___H2O
�ۼ���Cl���Ƿ�ϴ�Ӹɾ��ķ�����_______________��
��.��Ҫ����500mL 0.5mol��L-1��NaOH��Һ����ϴ������ش��������⣺
(3)����ʱ��Ӧ����ƽ��ȡNaOH������Ϊ___________(��ȷ��С�������λ)��
(4)ij����������ͼ��ʾ��
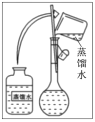
�ò���Ӧ������ͼ��ʾ��____________(�����)����֮�䡣
�� ��
��![]() ��
��![]() ��
��![]() ��
�� ��
��![]()
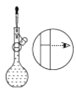
(5)����˵���������_____________(����)��
A.����NaOH�����ʱ�䲻�˹���
B.���ձ�����Һ��ȴ�����²Ž���ת��
C.����ʱ����������ƿ�̶���ʹ���Ƶ�NaOH��ҺŨ��ƫ��
D.����ƿ�ɴ����õ�NaOH��Һ
���𰸡�+3 �� 1 6 1 2 3 ȡ�������һ��ϴ��Һ���Թ��У�����ϡ��������ҺΪ���ԣ��ټ���������Һ�����ް�ɫ��������˵����ϴ�Ӹɾ� 10.00 g �ܢ� CD
��������
(1)���ݻ������и�Ԫ�ػ��ϼ۽��з������㣻
(2)�������ܽ�Ƚ��з�����
�ڸ��ݻ��ϼ�������ȣ������غ���д���ӷ���ʽ��
�����������ữ�����������飻
��3������m=cVM���м��㣻
(4)���ݲ���������з�����
(5)��������һ��Ũ����Һ������жϡ�
(1) FeOCl��OԪ��Ϊ-2�ۣ�ClԪ��Ϊ-1�ۣ����ݻ�����Ļ��ϼ۴����ܺ�Ϊ0�ɵ���Ԫ�صĻ��ϼ�Ϊ+3�ۣ�
(2)����Ϊ���ӷ�Ӧ�ı���������Ũ�ȵļ�С�����s(FeOCl)��s[FeO(OH)]��
�ڸ��ݻ��ϼ�������ȣ������غ���д���ӷ���ʽΪNa2SO3 +6FeO(OH) = Na2SO4 + 2Fe3O4 + 3H2O��
�ۼ��ϴ��Һ��Cl���ķ�����ȡ����ϴ��Һ���Թ��У�����ϡ��������ҺΪ���ԣ��ټ���������Һ�����ް�ɫ��������˵����ϴ�Ӹɾ���
��3�����������Ƶ�����Ϊm=0.5L��0.5molL-1��40g/mol=10.0g��
(4)ͼ�в����Ƕ��ݣ�����Ӧ��תҺ��ҡ��֮�䣬��Ӧ����ʾ�Ģܢݲ���֮�䣻
(5)A.��NaOH������ˮ����¶�ڿ����г���NaOH�����ʱ��̫�������ʵ�ʳƵõ�������������ƫС��������Һ��Ũ��ƫ�ͣ�ѡ��A��ȷ��
B. ĩ��ȴ�����¾�ת�ƽ�����ƿ���ᵼ����Һ�����ƫС����Һ��Ũ��ƫ�ʴ��ձ�����Һ��ȴ�����²Ž���ת�ƣ�ѡ��B��ȷ��
C.����ʱ����������ƿ�̶��ߣ�������Һ���ƫ��ʹ���Ƶ�NaOH��ҺŨ��ƫ�ͣ�ѡ��C����
D. ����ƿ�������ڱ�����ڴ��NaOH��Һ��ѡ��D����
��ѡCD��


 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵ���������ͭ�Ļ����24g��600mLϡ����ǡ����ȫ��Ӧ������NO6.72L����״��������Ӧ�����Һ�м���1molL-1NaOH��Һʹ��������ǡ�ó����������й�˵��������ǣ� ��
A.������ܽ�����Һ��c��Fe3+����c��Fe2+��=1��1
B.ϡ��������ʵ���Ũ�ȶ���2molL-1
C.��Ҫ����NaOH��Һ1000mL
D.������ó����ڿ����г�ּ��ȿɵù���32g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D�����л���������ת����ϵ�����ֲ����ת����������ȥ����

��֪ϩ��A������Ϊˮ���Ĵ������D��ʳ�ijɷ�֮һ��
��ش��������⣺
��1��д��B�����й����ŵ�����_________��
��2��A��һ����������ˮ��Ӧ�ܵõ�����B����û�ѧ��Ӧ�ķ�Ӧ������_____________��
��3��д����Ũ����������B��D��Ӧ�Ļ�ѧ����ʽ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
�������̼��Ԫ���ڿ���������������������й㷺��Ӧ�á��ش��������⣺
(1)��Ԫ�����ڱ��У���Li�Ļ�ѧ���������Ƶ�����Ԫ����__________(��Ԫ�ط���)����Ԫ�ػ�̬ԭ���������ӵ�����״̬___________(������ͬ�������෴��)��
(2)̼����йػ�ѧ������������ʾ��
��ѧ�� | C-H | C-O | Si-H | Si-O |
����/kJmol-1 | 413 | 336 | 318 | 452 |
SiH4���ȶ���С��CH4���������������ԭ����__________________��
(3)��Ȼ�����ζ�����[SiO4]�������Զ�����ԭ���������ɣ��ɳ���״Ҳ�ɳɻ������Թ���������ࡣ��ͼa����SiO44-��b��c�ǹ����������γɵĻ�״�ṹ��
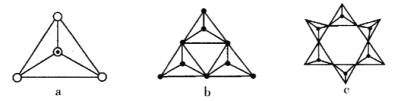
������������Si�Ĺ���ӻ�����Ϊ____________�� ͼb��״�ṹ������Ļ�ѧʽΪ______________���ڻ�״�ṹ�й��ԭ����Ϊn��д����״�ṹ�й������ͨʽ_____________��
(4)�������������γ��廯�ؾ��壬�þ�������Ϊ___________���侧���ܿ�ͨ����ͼ��Borm-Haberѭ������õ���
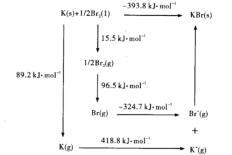
����ͼ��֪��Kԭ�ӵĵ�һ������Ϊ_____ kJ/mol�� Br-Br������Ϊ______kJ/ mol��KBr�ľ�����Ϊ______kJ/mol��������Խ�þ�����۵�Խ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� 4 molA�����3molB������2L�������л�ϲ���һ�������·������·�Ӧ��2A��g����B��g��![]() 2C��g��, ���� 2 s���� C��Ũ��Ϊ 0.6 molL-1���������м���˵����
2C��g��, ���� 2 s���� C��Ũ��Ϊ 0.6 molL-1���������м���˵����
��������A ��ʾ��Ӧ��ƽ������Ϊ 0.3 molL-1s-1
������ B�����������40%
��2 s ʱ���� A ��ת����Ϊ30��
��2 s ʱ���� B ��Ũ��Ϊ 1.0 molL-1
������ȷ����
A.�٢�B.�ڢ�C.�٢�D.�ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Fe��Cu��Cr���ǵ������ڹ���Ԫ�أ��ش��������⡣
��1��FeCl3��һ�ֳ��õľ�ˮ����ClԪ�ص�ԭ�Ӻ�����___�ֲ�ͬ�˶�״̬�ĵ��ӣ���___�ֲ�ͬ�ܼ��ĵ��ӣ���̬Fe3+�ĵ����Ų�ʽΪ___��
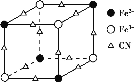
��2��ʵ�����п���KSCN��K4[Fe(CN)6]������Fe3+��FeCl3��KSCN��Һ��ϣ��ɵõ���λ��Ϊ5�������Ļ�ѧʽ��___��K4[Fe(CN)6]��Fe3+��Ӧ�ɵõ�һ����ɫ����KFe[Fe(CN)6]�������ʾ�����![]() �ṹ��ͼ��ʾ(K+δ����)����һ�������е�K+����Ϊ___��
�ṹ��ͼ��ʾ(K+δ����)����һ�������е�K+����Ϊ___��
��3��Cu2+�����Ҷ���(H2N��CH2��CH2��NH2)�γ���������ͼ��![]() �����������к��еĻ�ѧ��������___(����ĸ)��
�����������к��еĻ�ѧ��������___(����ĸ)��
a.��λ�� b.���Լ� c.���Ӽ� d.�Ǽ��Լ�
һ���Ҷ��������й���___��������Cԭ�ӵ��ӻ���ʽΪ___��
��4������ͭ�ľ���Ϊ�����������ܶѻ����߳�Ϊ361pm����ͭԭ�ӵ�ֱ��ԼΪ___pm��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������![]() ϡ��ˮ��
ϡ��ˮ��![]() ϡ����������ϣ������ж�һ����ȷ����
ϡ����������ϣ������ж�һ����ȷ����
A.��![]() ����
����![]() B.��
B.��![]() ����
����![]()
C.��![]() ����
����![]() D.��
D.��![]() ����
����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�pH���1������һԪ����ҺA��B���ֱ��ˮϡ��ʱ����Һ��pH�仯��ͼ��ʾ������˵����ȷ����( )
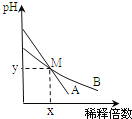
A.ϡ��ǰ��![]()
B.ϡ��ǰ��A��Һ����ˮ�������![]() ��Ũ�ȴ���
��Ũ�ȴ���![]()
C.�ô����к�A��Һ��ǡ����ȫ��Ӧʱ����Һ��pHΪ7
D.��M�㣬A��B���ּ���Һ�������ӵ����ʵ���Ũ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����VA��Ԫ�ص�ԭ��R��Aԭ�ӽ���γ�RA3��̬���ӣ�������ṹ�������Ρ�RCl5����̬��Һ̬ʱ�����ӽṹ����ͼ��ʾ�����й���RCl5���ӵ�˵������ȷ����

A.ÿ��ԭ�Ӷ��ﵽ8�����ȶ��ṹ
B.������5��R��Cl��������ͬ
C.����(Cl��R��Cl)��90����120����180������
D.RCl5���Ⱥ��ֽ����ɷ���RCl3��RCl5��RCl3���Ǽ��Է���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com