
| A. | ①③⑤⑦⑨ | B. | ②④⑧⑩ | C. | ①③ | D. | 全部 |
分析 ①纯净物是只含有一种物质的物质,只含有一种分子;
②混合物含有不同种分子,可能含有不同种类的原子也可能只含有一种原子;
③单质是由一种元素组成的纯净物;
④化合物是由两种或两种以上元素组成的纯净物;
⑤金属属于单质,只含有一种原子;
⑥非金属属于单质只含有一种原子;
⑦酸是电离时产生的氢离子和酸根离子的化合物;
⑧碱是电离时生成金属离子和氢氧根离子的化合物;
⑨盐电离时生成金属离子和酸根离子的化合物;
⑩氧化物是指由两种元素组成其中一种是氧元素的化合物.
解答 解:①纯净物是只含有一种物质的物质,只含有一种分子,可能含有不同种类的原子,也可能只含有一种原子,如HCl,Ne等物质;
②混合物含有不同种分子,可能含有不同种类的原子也可能只含有一种原子,如氧气和臭氧的混合物,氧气和氮气的混合物;
③单质是由一种元素组成的纯净物,一定含有一种原子,可以是相同原子可以是不同原子,如氢气:HD、DT等;
④化合物是由两种或两种以上元素组成的纯净物,一定含有不同种类的原子;
⑤金属属于单质,只含有一种相同原子;
⑥非金属属于单质只含有一种原子,如氢气:HD、DT等;
⑦酸是电离时产生的氢离子和酸根离子的化合物,含有不同种类的原子;
⑧碱是电离时生成金属离子和氢氧根离子的化合物,含有不同种类的原子;
⑨盐电离时生成金属离子和酸根离子的化合物,含有不同种类的原子;
⑩氧化物是指由两种元素组成其中一种是氧元素的化合物,含有不同种原子.
故选B.
点评 在熟悉概念的基础上能从宏观和微观两个方面来判断各类物质,注意同位素原子构成的单质分子是易错点,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 通入NO2:Na+、Fe2+、C1-、SO42- | B. | 通入NH3:AlO2-、NH4+、Na+、NO3- | ||
| C. | 通入Cl2:K+、NH4+、I-、C1- | D. | 通入CO2:Na+、K+、NO3-、SiO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | A | B | C | D | E |
| 硝酸溶液体积 | 100ml | 200mL | 300mL | 400mL | 500mL |
| 剩余固体的质量 | 17.2g | 8g | 0g | 0g | 0g |
| 气体体积 | 2.24L | 4.48L | 6.72L | 7.84L | 7.84L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 豆浆是胶体,因为豆浆中的分散质粒子直径在1nm~100nm之间 | |
| B. | NaCl溶液是电解质,因为NaCl溶液能导电 | |
| C. | Na和H2O的反应不是离子反应,因为反应中没有离子参加 | |
| D. | H2SO4是酸,因为H2SO4中含有氢元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
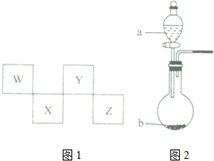 W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.
W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物. ,Z在周期表中的位置第三周期ⅦA族.
,Z在周期表中的位置第三周期ⅦA族.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.05 mol•L-1 | B. | 0.25 mol•L-1 | C. | 5 mol•L-1 | D. | 0.5 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 4:2:1 | C. | 2:3:4 | D. | 3:3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| A | B | C | D | |
| 物质 | 煤油 | 丙醇 | 四氯化碳 | 乙醚 |
| 沸点/℃ | 180~310℃ | 97.4 | 76.5 | 34.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol N2所含有的原子数为NA | |
| B. | 1mol•L-1 NaCl溶液中含有的钠离子数目为NA | |
| C. | 标准状况下,22.4 LCO所含的原子数为NA | |
| D. | 12.4g白磷(分子式为P4)中含有磷原子数为0.4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com