
 4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH
4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH  Fe3O4+2H2↑十4Na↑.下列有关说法正确的是( )
Fe3O4+2H2↑十4Na↑.下列有关说法正确的是( )
 4Na+O2↑+2H2O可知,阳极氢氧根离子放电生成氧气和水,电极反应为4OH--4e-=2H2O+O2↑,故A错误;
4Na+O2↑+2H2O可知,阳极氢氧根离子放电生成氧气和水,电极反应为4OH--4e-=2H2O+O2↑,故A错误; 4Na+O2↑+2H2O、3Fe+4NaOH
4Na+O2↑+2H2O、3Fe+4NaOH Fe3O4+2H2↑十4Na↑可知,戴维法生成4molNa转移4mol电子,但盖?吕萨克法生成4molNa转移8mol电子,则转移电子不等,故C错误;
Fe3O4+2H2↑十4Na↑可知,戴维法生成4molNa转移4mol电子,但盖?吕萨克法生成4molNa转移8mol电子,则转移电子不等,故C错误; 2Na+Cl2↑,故D正确;
2Na+Cl2↑,故D正确;

科目:高中化学 来源: 题型:
 (2013?闸北区二模)早在1807年化学家戴维用电解熔融氢氧化钠制得钠 4NaOH(熔)
(2013?闸北区二模)早在1807年化学家戴维用电解熔融氢氧化钠制得钠 4NaOH(熔) | 电解 |
| 1100℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为4NaOH(熔融)═4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH═Fe3O4+2H2↑+4Na↑.下列有关说法不正确的是( )
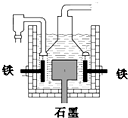
早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为4NaOH(熔融)═4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH═Fe3O4+2H2↑+4Na↑.下列有关说法不正确的是( )| A、电解熔融氢氧化钠制钠,阴极发生电极反应为:Na++e-═Na | B、盖?吕萨克法制钠原理是熵的增加带动了反应的进行 | C、若戴维法与盖?吕萨克法制得等量的钠,则两反应中转移的电子总数比为1:1 | D、目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 早在1807年化学家戴维用电解熔融氢氧化钠制得钠, 4NaOH(熔)
早在1807年化学家戴维用电解熔融氢氧化钠制得钠, 4NaOH(熔) ![]() 4Na + O2↑+ 2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:
4Na + O2↑+ 2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:
3Fe+4NaOH![]() Fe3O4+2H2↑十4Na↑。下列有关说法正确的是
Fe3O4+2H2↑十4Na↑。下列有关说法正确的是
A.电解熔融氢氧化钠制钠,阳极发生电极反应为:
2OH--2e-=H2↑+O2↑
B.盖·吕萨克法制钠原理是利用铁的还原性比钠强
C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数也相同
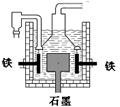
D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,
铁为阴极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com