
| A. | 配制盐酸用量筒量取盐酸时俯视刻度线 | |
| B. | 配制盐酸定容时,仰视容量瓶刻度线 | |
| C. | 称量20gNaOH来配制0.5 mol•L-1 NaOH溶液1000 mL 时,砝码错放在左盘 | |
| D. | NaOH溶解后未经冷却即注入容量瓶至刻度线 |
分析 A.俯视量筒刻度线导致量取盐酸的体积偏小,所配溶液浓度偏低;
B.定容时仰视容量瓶刻度线,导致液体体积偏大,所配溶液浓度偏低;
C.砝码错放在左盘,称量的氢氧化钠质量偏低,配制的溶液浓度偏低;
D.NaOH溶解后未经冷却即注入容量瓶至刻度线,导致溶液体积偏小,所配溶液浓度偏高.
解答 解:A.用量筒量取盐盐酸时,俯视刻度线导致量取盐酸的体积偏小,所配溶液中溶质的物质的量偏小,溶液浓度偏低,故A错误;
B.定容时仰视容量瓶刻度线,导致配制的盐酸体积偏大,所得溶液的浓度会偏低,故B错误;
C.称量氢氧化钠时砝码错放在左盘,导致称取的NaOH固体的质量偏小,配制的溶液浓度偏小,故C错误;
D.NaOH溶解后未经冷却即注入容量瓶至刻度线,导致所得溶液的体积偏小,所配溶液浓度偏高,故D正确;
故选D.
点评 本题考查了配制一定物质的量浓度的溶液方法及误差分析,题目难度不大,明确配制步骤为解答关键,注意掌握误差分析的方法与技巧,试题培养了学生的 化学实验能力.


 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 将SO2气体通入足量澄清石灰水 | |
| B. | 在Na2S溶液中通入SO2气体直至过过量 | |
| C. | 在Na2SO3溶液中通入H2S气体直至过量 | |
| D. | 将8.7克MnO2固体与含0.4mol溶质的浓盐酸加热并充分反应后 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁在氯气中燃烧,生成棕红色的烟 | |
| B. | 红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 | |
| C. | 纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现白色烟雾 | |
| D. | 氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
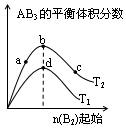 某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( )
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( )| A. | 图中T2一定大于T1 | |
| B. | 图中b点速率一定大于d点速率 | |
| C. | 达到平衡时,A2的转化率大小为:c>b>a | |
| D. | 加入催化剂可以使状态d变为状态b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com