
| 选项 | 实验 | 现象 | 解释或结论 |
| A | 用熔融AlCl3进行导电实验 | 无电流通过 | AlCl3是非电解质 |
| B | 向某溶液中滴加BaCl2溶液 | 产生白色沉淀 | 溶液中一定含有SO${\;}_{4}^{2-}$ |
| C | 把Cl2通入紫色石蕊试液中 | 紫色褪去 | Cl2具有漂白性 |
| D | 将滴有酚酞的碳酸钠溶液加热 | 红色变深 | 水解过程是吸热的 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.氯化铝为共价化合物,熔融氯化铝不导电;
B.生成的沉淀可能为氯化银、碳酸钡等,不一定为硫酸钡;
C.干燥的氯气不能使有色物质褪色,具有漂白性的是次氯酸,氯气不具有漂白性;
D.碳酸根离子水解溶液呈碱性,加热后溶液变深,说明碳酸根离子的水解程度增大,从而证明水解共存吸热.
解答 解:A.氯化铝为共价化合物,在溶液中能够导电,而用熔融AlCl3进行导电实验时不会导电,氯化铝为电解质,故A错误;
B.向某溶液中滴加BaCl2溶液,产生的沉淀可能为氯化银、亚硫酸钡、碳酸钡等,不一定为硫酸钡,原溶液中可能含有银离子、碳酸根离子,不一定含有硫酸根离子,故B错误;
C.把Cl2通入紫色石蕊试液中,氯气与水反应生成的次氯酸具有漂白性,所以溶液褪色,而氯气不具有漂白性,故C错误;
D.将滴有酚酞的碳酸钠溶液加热,红色变深,说明碳酸根离子的水解程度增大,证明了水解过程是吸热的,故D正确;
故选D.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及离子检验、氯气化学性质、电解质与非电解质的判断、水解反应等知识,明确常见元素及其化合物性质为解答关键,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 47 | B. | 175 | C. | 61 | D. | 57 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
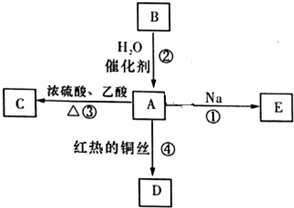 A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,能进行如图所示的多种反应.
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,能进行如图所示的多种反应. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
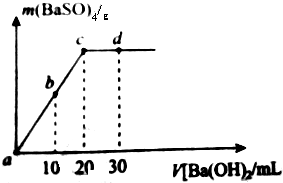 室温下,向20m1,物质的量浓度为0.35mol/L的H2SO4溶液中逐滴加人浓度的Ba(OH)2溶液,生成的沉淀与加人Ba(OH)2的体积如图(混合后体积变化忽略不计)下列说法不正确的是( )
室温下,向20m1,物质的量浓度为0.35mol/L的H2SO4溶液中逐滴加人浓度的Ba(OH)2溶液,生成的沉淀与加人Ba(OH)2的体积如图(混合后体积变化忽略不计)下列说法不正确的是( )| A. | Ba(OH)2的物质的量浓密度为0.35mol/L | |
| B. | b时刻溶液中SO${\;}_{4}^{2-}$的浓度约为0.175mol/L | |
| C. | c时刻溶液显中性 | |
| D. | 实验过程中a、b、c三处溶液的导电能力c<b<a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cn元素的相对原子质量为277 | |
| B. | 277112Cn的原子核内中子数比质子数多53 | |
| C. | 上述合成过程中属于化学变化 | |
| D. | Cn元素位于元素周期表的第六周期,是副族元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com